
| A.X+32 | B.X+4 | C.X+8 | D.X+18 |
 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源:不详 题型:单选题
| A.由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 |
| B.YX3的水溶液呈弱碱性,能使湿润的蓝色石蕊试纸变红 |
| C.原子半径:Z<Y<W,而简单离子半径:W<Y<Z |
| D.W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
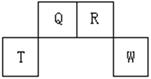
| | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.6 | 0.75 | 0.82 |
| 最高或最低化合价 | | +2 | +1 | +5 | +7 | +1 | +5 | +3 |
| -2 | | | -3 | -1 | | -3 | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铊是易导电的银白色金属 | B.铊能生成+3价的离子 |
| C.Tl3+的氧化能力比Al3+强 | D.氢氧化铊的碱性比氢氧化铝强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氮化镓是由主族元素与副族元素形成的化合物 | B.氮化镓能把白铁变成黄金 |
| C.氮化镓中氮元素显+3价 | D.氮原子最外层比镓原子最外层多2个电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com