
| A. | Al、Si、P | B. | I、Br、Cl | C. | O、S、Na | D. | Na、Mg、Ba |
分析 电子层数越多,半径越大;
当电子层数相同时,核电荷数越大,半径越小;
当电子层数相同、核电荷数也相同时,核外电子数越多,半径越大,据此分析.
解答 解:A、Al、Si、P的电子层数相同,但核电荷数逐渐增大,故半径逐渐减小,故A错误;
B、I、Br、Cl的电子层数逐渐减小,故半径逐渐减小,故B错误;
C、O的电子层数小于S和Na的电子层数,故O的半径最小;而S和Na的电子层数相同,而Na的核电荷数比S小,故半径比S大,故O、S、Na的半径逐渐增大,故C正确;
D、Na、Mg的电子层数均比Ba的小,故Ba的半径最大;而Na和Mg的电子层数相同,而Na的核电荷数比Mg小,故Na的半径比Mg大,故其中Mg的半径是最小的,故D错误.
故选C.
点评 本题考查了微粒半径的大小比较,难度不大,应注意从电子层数、核电荷数和电子数的顺序来考虑.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:解答题
 .
.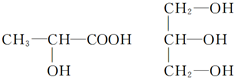
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2.4g 金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1mol甲烷分子所含质子数为10NA | |
| C. | 常温常压下,2g氢气含有的分子与32g氧气中分子数目均为NA | |
| D. | 4g氦气所含原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为 COOH的异构体共有7种,其中的3种是:
COOH的异构体共有7种,其中的3种是: CH2CH2CH2CH2CH3,
CH2CH2CH2CH2CH3,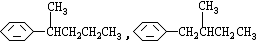
 ,
,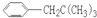 ,
,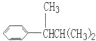 ,
,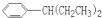 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| I1 | I2 | I3 | I4 | |
| 电离能(kJ•mol-1) | 578 | 1 817 | 2 745 | 11 578 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )
曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )| A. | 盐酸的物质的量浓度与 NaOH 溶液的物质的量浓度相等 | |
| B. | P 点时溶液中 c(Na+)=c(Cl-)=c(H+)=c(OH-) | |
| C. | 曲线 a 是盐酸滴定氢氧化钠溶液的滴定曲线 | |
| D. | 曲线 b 中滴定前 NaOH 溶液的体积为 150 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
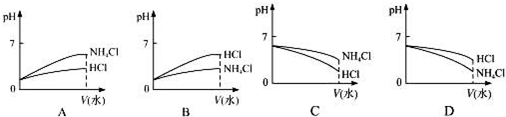
| 实验编号 | 氨水物质的量浓度/ (mol•L-1) | 盐酸物质的量浓度/ (mol•L-1) | 混合溶液pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23gNa在氧气中完全燃烧失去NA个电子 | |
| B. | 常温常压下,6.2g Na2O含有的Na+离子数为0.2 NA | |
| C. | 标准状况下,22.4LH2O含有NA个分子 | |
| D. | 1L0.5 mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com