
下列电离方程式正确的是()
A. MgSO4=Mg2++SO42﹣ B. Ba(OH)2=Ba2++OH﹣
C. Al2(SO4)3=2Al+3+3SO42﹣ D. KClO3=K++Cl﹣+3O2﹣
考点: 电离方程式的书写.
专题: 电离平衡与溶液的pH专题.
分析: 用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式.离子所带电荷数一般可根据它们在化合物中的化合价来判断.所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等.
解答: 解:A、MgSO4=Mg2++SO42﹣,电荷守恒、离子符号正确,所以电离方程式书写正确,故A正确;
B、正确的书写为:Ba(OH)2=Ba2++2OH﹣,电荷不守恒,故B错误;
C、A12(S04)3═2A13++3S042﹣,离子符号书写不正确,故C错误;
D、含有原子团的物质电离时,原子团应作为一个整体,不能分开,氯酸根不能分,故D错误.
故选A.
点评: 掌握正确书写电离方程式的方法,并会正确判断离子方程式的正误是考试的热点,难度不大.


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:高中化学 来源: 题型:
铝土矿(主要成分为Al2O3,还有少量杂质)是提取氧化铝的原料。提取氧化铝的工艺流程如下:

(1)请用离子方程式表示以上工艺流程中第①步反应:___________________ 。
(2)写出以上工艺流程中第③步反应的化学方程式:_______________________。
(3)金属铝与氧化铁混合点燃,会发生剧烈的反应。该反应的化学方程式为 __
________________________________________________________________。
请举一例该反应的用途______________________________________________。
(4)电解熔融氧化铝制取金属铝,若有0.6 mol电子发生转移,理论上能得到金属铝的质量是 ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电化学知识,自己动手设计一个电池。请填写下列空白:
(1)实验原理:Fe+2H+===Fe2++H2↑
(2)实验用品:电极(________、________)、稀硫酸、________、________、耳机(或者电流计)(填写所缺的实验用品)。
(3)实验装置如图。
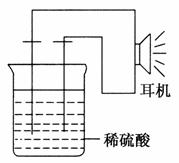
(4)原电池设计及注意的问题:
①按如图所示装置连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一极是连接在原电池的另一个电极上的),这时可以听见耳机发生“嚓嚓嚓……”的声音。其原因是在原电池中,化学能转化为________,在耳机中又由________转化为声音这种能量。
②如果将装置中的耳机改为电流计,则________应该接电流计的负极,电极反应是________,发生了________反应;________应该接电流计的正极,电极反应是________,发生了________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,离子方程式正确的是()
A. 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
B. 碳酸钙跟盐酸反应:CO32﹣+2H+=H2O+CO2↑
C. 稀硫酸跟氢氧化钾溶液反应:H++OH﹣═H2O
D. 氢氧化钡溶液跟稀硫酸反应:Ba2++SO42﹣═BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
除去粗盐中的Ca2+、Mg2+、SO42﹣以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
称取粗盐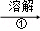
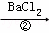
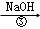
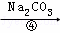
 滤液
滤液 
 粗盐
粗盐
(1)判断BaCl2已过量的方法是继续滴加氯化钡溶液不再出现沉淀.
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)l.
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是在..
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com