
【题目】探究![]() 反应的速率影响因素,设计了以下实验。下列说法正确的是
反应的速率影响因素,设计了以下实验。下列说法正确的是
锥形瓶标号 |
| 蒸馏水 |
| 反应温度 | 浑浊出现时间 | 备注 |
1 |
| 0 mL | 10 mL |
| 10s | |
2 | 10mL | 5mL | 5 mL |
| 16 s | |
3 | 10mL | 0mL | 10 mL |
| 5 s | 第10s开始浑浊不再增多 |
4 | 10mL | 6mL | 4mL |
| 8s |
A.该反应也可通过测![]() 的体积变化来表示化学反应速率的快慢
的体积变化来表示化学反应速率的快慢
B.3号瓶用![]() 来表示速率为
来表示速率为![]()
C.由2号瓶和3号瓶实验结果可得温度越高反应速率越快
D.由1号瓶和4号瓶实验结果可得温度越高反应速率越快
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。
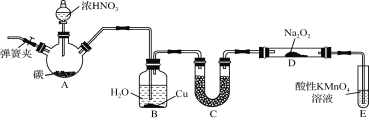
【背景素材】
①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO![]() ,MnO
,MnO![]() 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2;S2O32-能把I2还原为I-。
【制备NaNO2】
(1) 装置A三颈烧瓶中发生反应的化学方程式为 。
(2) B装置的目的是① ,② 。
(3) 为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是 (填序号)。
A. P2O5 B. 碱石灰 C. 无水CaCl2 D. 生石灰
(4) E装置发生反应的离子方程式是 。
【测定NaNO2纯度】
(5) 本小题可供选择的试剂有:
A.稀硫酸
B.c1mol·L-1KI溶液
C.淀粉溶液
D.c2mol·L-1Na2S2O3溶液
E.c3mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,可选择的试剂是 (填序号)。
②利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解 (请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在化学反应中使普通分子变成活化分子所需提供的最低能量叫活化能,观察如图,然后回答问题。

①图中反应是___(填“吸热”或“放热”),该反应的△H=___(用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+![]() O2(g)=H2O(g) △H=-241.8kJmol-1,该反应的活化能为167.2kJmol-1,则其逆反应的活化能为___。
O2(g)=H2O(g) △H=-241.8kJmol-1,该反应的活化能为167.2kJmol-1,则其逆反应的活化能为___。
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.0kJ的热量。
①反应的热化学方程式为___。
②又已知H2O(l)=H2O(g);ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出热量是___kJ。
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用高分子吸附树脂提取卤水中的碘(主要以 I-形式存在)的工艺流程如下,说法不正确的是
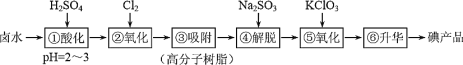
A.流程②的反应说明 I 的非金属性弱于 Cl
B.经①和④所得溶液中,I-的浓度后者大于前者
C.氯元素的相对原子质量是 35.5, 则存在的 35Cl 、37Cl 的丰度比约为 3:1
D.若在流程②和⑤中要得到等量的 I2,则需消耗的 n(Cl2) :n(KClO3) = 5:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是

A. 原子半径:Y>Z>W
B. 单质的还原性:X>Y
C. 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D. 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应叙述相符的是
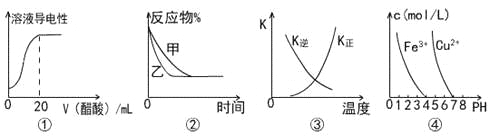
A.图①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液导电性随加入酸体积的变化
B.图②表示压强对可逆反应A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图③中曲线表示反应3A(g) + B(g)![]() 2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
D.据图④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车发动机中生成NO的反应为:![]() ,
,![]() 时该反应的化学平衡常数
时该反应的化学平衡常数![]() 。在
。在![]() 下甲、乙、丙三个恒容密闭容器中,投入
下甲、乙、丙三个恒容密闭容器中,投入![]() 和
和![]() 模拟反应,起始浓度如下表所示。下列判断不正确的是.
模拟反应,起始浓度如下表所示。下列判断不正确的是.
起始浓度 | 甲 | 乙 | 丙 |
|
|
|
|
|
|
|
|
A.起始时,反应速率:丙![]() 甲
甲![]() 乙
乙
B.平衡时,![]() :甲
:甲![]() 丙
丙![]() 乙
乙
C.平衡时,![]() 的转化率:甲
的转化率:甲![]() 乙
乙
D.平衡时,甲中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2020年抗击新型冠状病毒肺炎的战役中,化学药品发挥了重要作用。下列说法不正确的是( )
A.84消毒液、过氧乙酸溶液均可作为环境消毒剂
B.医用消毒酒精中乙醇的体积分数为75%
C.用来合成抑制新冠病毒(COVID-19)的潜在药物磷酸氯喹的中间体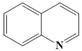 (喹啉)属于芳香烃
(喹啉)属于芳香烃
D.生产医用防护口罩的原料聚丙烯纤维属于有机高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定镁带在空气中完全燃烧后所得固体产物![]() 假设只含MgO、
假设只含MgO、![]() 的组成,某同学称取
的组成,某同学称取![]() 固体进行如下实验
固体进行如下实验![]() 室温
室温![]() :
:
![]()
已知:![]()
下列说法错误的是
A.![]() 不能存在于水中
不能存在于水中
B.固体中![]()
C.溶液X中存在![]()
D.![]() 等于
等于![]() 时,溶液X中的
时,溶液X中的![]() 恰好沉淀完全
恰好沉淀完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com