
| A、5mol/L |
| B、6mol/L |
| C、6.25mol/L |
| D、6.75mol/L |
| m |
| M |
| n |
| V |
| (200-100)g×28% |
| 56g/mol |
| 0.5mol |
| 0.08L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、CO2通入饱和Na2CO3溶液中 |
| B、CO2通入CaCl2溶液中 |
| C、SO2通入澄清石灰水中 |
| D、H2S通入SO2的水溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是表示物质的量的单位 |
| B、胶体区别于溶液本质是胶体的分散质粒子直径在1 nm~100nm之间 |
| C、氧化还原反应的实质是电子的得失或电子对偏移 |
| D、每次做焰色反应实验后都要用Na2CO3溶液来清洗铂丝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaSO3 |
| B、SO2 |
| C、SO3 |
| D、CaS |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、几千万年前地球上一条恐龙体内的某个原子可能在你的身体里 |
| B、在化学变化中,分子可以再分,离子和原子不可以再分 |
| C、一定条件下,金属钠可以成为绝缘体 |
| D、一定条件下,水在20℃时能凝固成固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
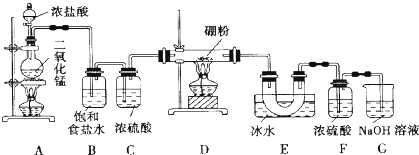
查看答案和解析>>
科目:高中化学 来源: 题型:
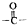 c.-CHO
c.-CHO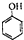 和
和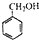 可用的试剂是
可用的试剂是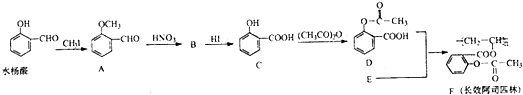
查看答案和解析>>
科目:高中化学 来源: 题型:
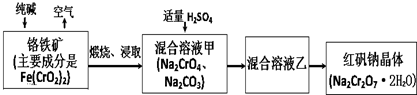
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com