
等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5︰6,则甲、乙两烧杯中的反应情况可能分别是( )
A. 甲、乙中都是铝过量 B. 甲中铝过量、乙中碱过量
C. 甲中酸过量、乙中铝过量 D. 甲中酸过量、乙中碱过量
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
某学生为探究钠与CO2的反应,利用如下装置进行实验。(已知PdCl2能被CO还原得到黑色的Pd)。可供选择的药品有:CaCO3(块状)、Na2CO3(粉末)、盐酸、稀硫酸、钠。
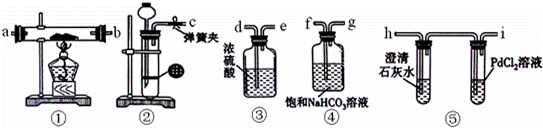
(1)请将上图各装置连接完整:②→ → →①→ 。(填装置序号)
(2)装置②有孔塑料板上所放的药品是: 。
(3)检查装置气密性并装好药品后,当观察到 现象时才点燃酒精灯,此步骤操作的目的是 。
(4)已知CO在潮湿环境中可将PdCl2还原为黑色粉末状的钯(Pd),写出该反应的化学方程式 。
(5)实验过程中CO2足量,装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。据此现象写出Na与CO2反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应中,不属于四种基本反 应类型的是( )。
应类型的是( )。
A.2FeCl3+Cu=2FeCl2+CuCl2 B.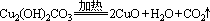
C.4Fe(OH)2+O2+2H2O= 4Fe(OH)3 D.CaCO3+2HCl=CaCl2+H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 == 3Cu(NO3)2 + 2NO↑+ 4H2O
⑴用双线桥法分析上述反应(只需标出电子得失的方向和数目)
⑵上述反应中氧化剂是  ,氧化产物是 。硝酸没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸占总硝酸的 。
,氧化产物是 。硝酸没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸占总硝酸的 。
查看答案和解析>>
科目:高中化学 来源: 题型:
只用试管和胶头滴管而不用其它试剂无法区分的一组溶液是( )
A.KOH溶液和AlCl3溶液 B.Na2CO3溶液和盐酸
C.MgCl2溶液和 氨水 D.盐酸和NaAlO2溶液
氨水 D.盐酸和NaAlO2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或氢气,或一氧化碳)法;③活泼金属置换法;④电解法。四种方法在工业上均有应用。古代有(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜;现代有(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁,对它们的冶炼方法的分析不正确的是( )
A.(Ⅰ)用① B.(Ⅱ)用② C.(Ⅲ)用③ D. (Ⅳ)用④
(Ⅳ)用④
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是
A.Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O
B.等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓
C.将过量的SO2通入Ca(ClO)2溶液中: SO2+ClO-+H2O =HClO+ HSO3-
D.将0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合:
2Al3++3SO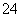 +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,某反应的化学方程式为:CO2+NO  NO2+CO ,下列说法正确的是( )
NO2+CO ,下列说法正确的是( )
A.升高温度,正反应速率增大,逆反应速率减少
B.恒温时,压缩容器的体积,颜色加深,因平衡左移
C.达到平衡,其平衡常数为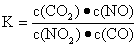
D.恒容时,升高温度,混合气体的颜色加深,该反应的焓变为正值
查看答案和解析>>
科目:高中化学 来源: 题型:
对于溶液中某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入足量稀盐酸,再加入氯化钡溶液后有白色沉淀产生,一定有SO42-
D.加入碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,一定有Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com