
 (2012?济南一模)(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100℃时1mol?L-1 的NaOH溶液中,由水电离出的c(H+)=
(2012?济南一模)(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度.100℃时1mol?L-1 的NaOH溶液中,由水电离出的c(H+)=| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×l0-10 |
| CH3COOH | K=1.8×l0-5 |
| H2CO3 | K1=4.3×l0-7、K2=5.6×l0-11 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
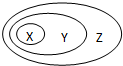 (2012?济南一模)下表所列物质或概念间的从属关系符合如图所示关系的是( ) (2012?济南一模)下表所列物质或概念间的从属关系符合如图所示关系的是( )
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com