
| A、PCl3→PCl5 |
| B、MnO4-→Mn2+ |
| C、SO3→SO42- |
| D、CO2→CO32 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HC≡CH |
| B、CH2=CH2 |
| C、HC≡C-CH3 |
| D、CH2=C(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
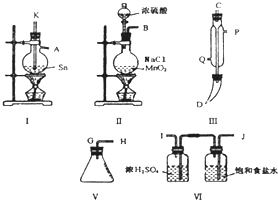 四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃,拟利用图中的仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热).请回答下列各问题.
四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃,拟利用图中的仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热).请回答下列各问题.查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是( )
室温下,用0.100mol/L 盐酸溶液滴定20.00mL 0.100mol/L的某氨水溶液,滴定曲线如图所示,下列有关说法不正确的是( )| A、曲线上除d点外任意一点所示溶液中:c(NH4+)+c(H+)=c(Cl- )+c(OH - ) |
| B、a点所示溶液中,c(Cl-)>c(NH4+ )>c(NH3?H2O)>c(OH- )>c(H+ ) |
| C、b点所示溶液中,c(NH4+)=c(Cl-) |
| D、c点所示溶液中,c(Cl- )>c(NH4+)>c(H+)>c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水煤气是二次能源 |
| B、水力是二次能源 |
| C、天然气是二次能源 |
| D、电能是一次能源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com