
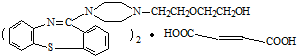 ,它的合成路线如下:
,它的合成路线如下: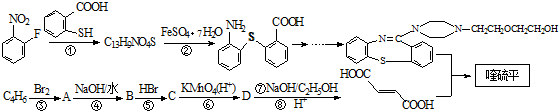
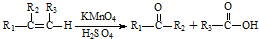
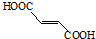 含有的官能团名称为碳碳双键和羧基.
含有的官能团名称为碳碳双键和羧基.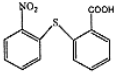 .
.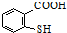 在一定条件下发生缩聚反应的化学方程式为
在一定条件下发生缩聚反应的化学方程式为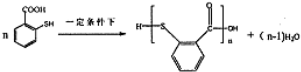 .
. 是一种重要的有机化合物.请设计合理方案,完成从
是一种重要的有机化合物.请设计合理方案,完成从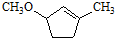 到
到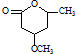 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用). 分析 A的系统命名为1,4-二溴-2-丁烯,则A结构简式为:BrCH2CH=CHCH2Br,则C4H6为CH2=CH-CH2=CH2;A与氢氧化钠的水溶液加热生成B,则B为HOCH2CH=CHCH2OH;B与HBr生成C,则C为HOCH2CH2CHBrCH2OH;C被酸性高锰酸钾溶液氧化成D:HOOCCH2CHBrCOOH,D在氢氧化钠的醇溶液中加热发生消去反应生成E:HOOCCH=CHCOOH;反应①为取代反应,则结合反应②的产物可知分子式为C13H9NO4S的物质的结构简式为: ,
,
(6)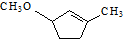 和水发生加成反应生成
和水发生加成反应生成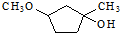 ,
, 发生消去反应生成
发生消去反应生成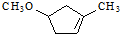 ,
, 被酸性高锰酸钾溶液氧化得到,据此
被酸性高锰酸钾溶液氧化得到,据此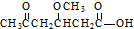 ,
,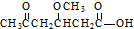 和氢气发生催化加成反应生成CH3CH(OH)CH2CH(OCH3)CH2COOH,最后发生酯化反应生成
和氢气发生催化加成反应生成CH3CH(OH)CH2CH(OCH3)CH2COOH,最后发生酯化反应生成 ,分析解答.
,分析解答.
解答 解:A的系统命名为1,4-二溴-2-丁烯,则A结构简式为:BrCH2CH=CHCH2Br,则C4H6为CH2=CH-CH2=CH2;A与氢氧化钠的水溶液加热生成B,则B为HOCH2CH=CHCH2OH;B与HBr生成C,则C为HOCH2CH2CHBrCH2OH;C被酸性高锰酸钾溶液氧化成D:HOOCCH2CHBrCOOH,D在氢氧化钠的醇溶液中加热发生消去反应生成E:HOOCCH=CHCOOH;反应①为取代反应,则结合反应②的产物可知分子式为C13H9NO4S的物质的结构简式为: ,
,
(1)物质  含有的官能团名称为羧基、碳碳双键,故答案为:碳碳双键和羧基;
含有的官能团名称为羧基、碳碳双键,故答案为:碳碳双键和羧基;
(2)分子式为C13H9NO4S的物质的结构简式是 ,故答案为:
,故答案为: ;
;
(3)反应⑤的目的是保护碳碳双键,防止被酸性高锰酸钾溶液氧化,故答案为:保护碳碳双键,防止被酸性高锰酸钾溶液氧化;
(4)B为HOCH2CH=CHCH2OH,物质B的同分异构体符合下列条件,
①能发生银镜反应,说明含有醛基;
②与NaOH能反应,与NaHCO3不反应,说明含有醇羟基或酯基;
③核磁共振氢谱只有三个峰,说明只含三种氢原子,
符合条件的物质结构简式为HCOOCH(CH3)2,
故答案为:HCOOCH(CH3)2;
(5)SH(巯基)的性质与-OH相似,则 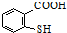 在一定条件下发生缩聚反应的化学方程式为:
在一定条件下发生缩聚反应的化学方程式为: ,
,
故答案为: ;
;
(6) 和水发生加成反应生成
和水发生加成反应生成 ,
, 发生消去反应生成
发生消去反应生成 ,
, 被酸性高锰酸钾溶液氧化得到,据此
被酸性高锰酸钾溶液氧化得到,据此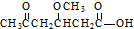 ,
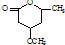
,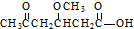 和氢气发生催化加成反应生成CH3CH(OH)CH2CH(OCH3)CH2COOH,最后发生酯化反应生成
和氢气发生催化加成反应生成CH3CH(OH)CH2CH(OCH3)CH2COOH,最后发生酯化反应生成 ,所以其合成路线为
,所以其合成路线为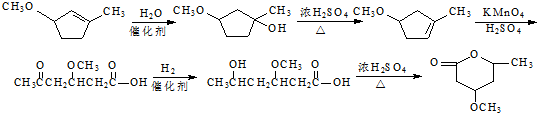 ,
,
故答案为: .
.
点评 本题考查有机物推断及有机物合成,为高频考点,侧重考查学生的分析、理解能力及综合应用所学知识的能力,根据某些物质结构简式、有机物的官能团及其性质结合反应条件进行推断,难点是有机合成路线设计,需要学生掌握有机物官能团性质、有机反应条件并灵活运用,题目难度中等.


 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 | |
| B. | 在沸腾的蒸馏水中滴加饱和FeCl3溶液,制Fe(OH)3胶体 | |
| C. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| D. | 用排饱和食盐水的方法收集氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都具有脱水性 | |
| B. | 在加热条件下都能与碳反应 | |
| C. | 露置于空气中都能形成白雾 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验①中产生的气体为氨气,并可得原溶液中c(NH4+)=0.1 mol•L-1 | |
| B. | 实验③中的沉淀中一定有BaSO4,可能有Mg(OH)2 | |
| C. | 若要判断原溶液中是否有Cl-,无需另外设计实验验证 | |
| D. | 原溶液中一定有K+,且c(K+)≥0.4 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com