
| A. | HCl | B. | CH3Cl | C. | CHCl3 | D. | CCl4 |
分析 CH4与Cl2发生取代反应,每生成1mol氯代烷,可生成1molHCl,CH4与Cl2发生的每一步取代反应中都有HCl生成,据此解答.
解答 解:由CH4和氯气发生取代反应的化学方程式可以知道,每生成1mol氯代烷,可生成1molHCl,由于CH4和Cl2发生的每一步取代反应中都有HCl生成,不要错误地认为n(CH4):n(Cl2)=1:1,则按下式进行反应:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,不再发生其它反应,其实,该反应一旦发生,生成的CH3Cl与Cl2发生“连锁”反应,所以生成的HCl的物质的量最多,
故选:A.
点评 本题考查了甲烷的性质,熟悉取代反应的原理和特点是解题关键,题目难度不.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NCl3的电子式: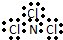 | B. | H- 的结构示意图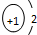 | ||
| C. | 含有4个中子的锂原子:74Li | D. | 次氯酸的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
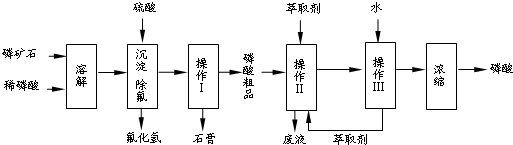
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 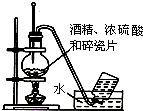 实验室用乙醇制取乙烯 | B. |  实验室制取乙酸乙酯 | ||
| C. | 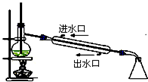 石油分馏 | D. | 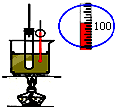 实验室制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
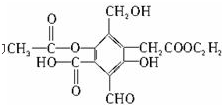
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com