
【题目】工业上以废铜为原料经一系列化学反应可生产氯化亚铜(CuCl),其工艺流程如下图所示:
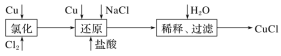
试依据如图转化回答下列问题:
(1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液吸收的原因是_______。
(2)还原过程中的产物为Na[CuCl2],试写出该反应的化学方程式:___________。
(3)合成结束后所得产品用酒精淋洗的目的是_______________。
(4)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,试写出该反应的离子方程式:____。
【答案】石灰乳来源丰富,成本低,且反应结束后可得副产品漂白粉 CuCl2+2NaCl+Cu=2Na[CuCl2] 使CuCl尽快干燥,防止被空气氧化 2Cu2++2Cl-+SO2+2H2O ![]() 2CuCl↓+4H++SO42—
2CuCl↓+4H++SO42—
【解析】
(1)工业生产Cl2时,尾气常用石灰乳吸收,而不用烧碱溶液,可从成本和产品两个方面考虑,从而得出这样操作的原因是石灰乳来源丰富,成本低,且反应结束后可得副产品漂白粉。答案为:石灰乳来源丰富,成本低,且反应结束后可得副产品漂白粉
(2)还原过程中的产物为Na[CuCl2],反应的化学方程式:CuCl2+2NaCl+Cu=2Na[CuCl2]。答案为:CuCl2+2NaCl+Cu=2Na[CuCl2]
(3)若用水洗,后续操作为烘干;若用酒精洗涤,固体表面的酒精自然挥发,不需烘干。因为氯化亚铜性质不稳定,烘干时易被空气中的氧气氧化,所以合成结束后所得产品应用酒精淋洗。答案为:使CuCl尽快干燥,防止被空气氧化
(4)实验室中在CuCl2热溶液中通入SO2气体也可制备白色的CuCl沉淀,该反应的离子方程式:2Cu2++2Cl-+SO2+2H2O ![]() 2CuCl↓+4H++SO42—。
2CuCl↓+4H++SO42—。
答案为:2Cu2++2Cl-+SO2+2H2O ![]() 2CuCl↓+4H++SO42—
2CuCl↓+4H++SO42—


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中 加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1))中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )

A. 2NO2![]() N2O4是放热反应
N2O4是放热反应
B. NH4Cl溶于水时放出热量
C. 烧瓶(1)中平衡混合气的平均相对分子质量增大
D. 烧瓶(3)中气体的压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备Cl2通常采用如图所示装置:

(1)A装置中发生反应的化学方程式是________;其中氧化剂是_________,每生成1 mol Cl2,被氧化的物质的物质的量是_____mol。
(2)仪器a的名称是_________;
(3)B装置中所盛的试剂是________________,装置C的作用是________________;
(4)若将下图集气瓶中充满饱和食盐水,代替装置D收集氯气,此时应气体从_______口流入(填“A”或“B”)。
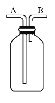
(5)E装置中发生反应的化学方程式是________________________。
(6)将下图装置代替装置D和E,可进行“氯气与金属钠反应”的实验,以下叙述正确的是________。
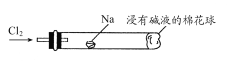
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气
C.玻璃管中,钠燃烧时会产生苍白色火焰
D.若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法正确的是
A.古代造纸工艺中使用的明矾易导致纸张发生酸性腐蚀
B.食用花生油、葡萄糖和鸡蛋清均能发生水解反应
C.用活性炭去除冰箱中异味的过程属于化学变化
D.天然气、液化石油气和煤是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.将少量饱和氯化铁溶液滴入沸水中,继续煮沸,可制得Fe(OH)3胶体,反应的方程式为:FeCl3 + 3H2O ![]() Fe(OH)3(胶体) + 3HCl
Fe(OH)3(胶体) + 3HCl
(1)当溶液呈________时,停止加热,即制得Fe(OH)3胶体。
(2)氢氧化铁胶体与氢氧化铁沉淀的本质区别是____________________。
(3)下列叙述错误的是________。
A.雾属于胶体,能产生丁达尔效应
B.从颜色上无法区别FeCl3溶液和Fe(OH)3胶体
C.明矾可以用于净水,净水原理和胶体有关
D.用盐卤点豆腐与胶体性质有关
Ⅱ.有A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是NO3-、SO42-、Cl-、CO32-中的一种(离子在物质中不重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。请回答下列问题:
(4)A的化学式为____________,B的化学式为____________。
(5)写出D与足量CH3COOH溶液反应的离子方程式_____________________________。
(6)写出A溶液中阴离子的检验方法______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾的生产流程如图,涉及的离子反应方程式书写错误的是( )
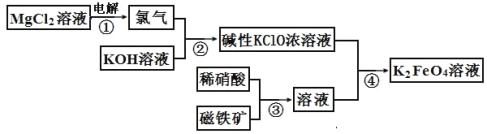
A. 2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B. Cl2+2OH-=Cl-+ClO-+H2O
C. 3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O
D. 2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中a、b、c表示相应仪器中加入的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | NO2 | 浓硝酸 | 铜屑 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型锰氢二次电池原理如图所示。该电池以MnSO4溶液为电解液,碳纤维与Pt/C分别为电极材料,电池的总反应为Mn2++ 2H2O![]() MnO2 + 2H++ H2↑。下列说法错误的是
MnO2 + 2H++ H2↑。下列说法错误的是
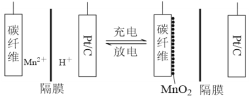
A. 充电时,碳纤维电极做阳极
B. 充电时,碳纤维电极附近溶液的pH增大
C. 放电时,电子由Pt/C电极经导线流向碳纤维电极
D. 放电时,正极反应式为MnO2 + 4H++ 2e-=Mn2++ 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHISO4溶于水时电离出Na+、H+、SO42-,某同学欲探究其化学性质,称取了12.0g NaHSO4,固体配成100mL溶液,做了如下实验:
①取20 mL该溶液加入足量Zn粒有大量气体生成;
②取20 mL该溶液加入Fe2O3后溶液变黄色;
③取20 mL该溶液加入BaCl2溶液后有大量白色沉淀产生。
请回答下列问题:
(1)该实验所配置的NaHSO4溶液物质的量浓度为__________。
(2)请用离子方程式解释①中的实验现象___________,该实验过程中产生的气体体积为__________(请按标准状况下计算)。
(3)请用离子方程式解释②中的实验现象_________________。
(4)请用离子方程式解释③中的实验现象__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com