
 �״�����Ϊ21���͵�����ȼ�ϣ���ҵ����CH4��H2OΪԭ��ͨ�����з�Ӧ�ٺ͢ڣ����Ʊ��״���
�״�����Ϊ21���͵�����ȼ�ϣ���ҵ����CH4��H2OΪԭ��ͨ�����з�Ӧ�ٺ͢ڣ����Ʊ��״���
��CH4(g)+H2O(g)![]() CO(g)+3H2(g) DH1
CO(g)+3H2(g) DH1
��CO(g)+2H2(g)![]() CH3OH(g) DH2
CH3OH(g) DH2
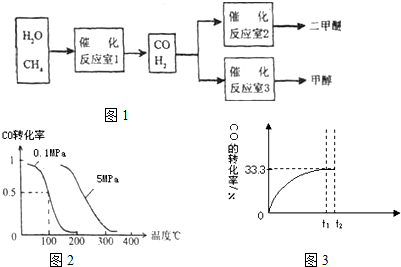
��0.20 mol CH4��0.30 mol H2O(g)ͨ���ݻ�Ϊ10 L���ܱ������У���һ�������·�����Ӧ�٣��ﵽƽ��ʱ��CH4��ת�������¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��
���¶Ȳ��䣬��С������ٵ��淴Ӧ���� (���������С�����䡱)��
�Ʒ�Ӧ�ٵ�DH1 0(�������=������)100��Cʱ��ƽ�ⳣ��ֵK= ��
����ѹǿΪ0.1Mpa�����£���amolCO��3amolH2�Ļ�������ڴ��������½��з�Ӧ�������ɼ״���Ϊ�˷�Ѱ�Һϳɼ״������˵��¶Ⱥ�ѹǿ��ijͬѧ����˶���ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ��С����ڿո�������ʣ���ʵ���������ݡ�
| ʵ���� | T(��C) | n(CO)/n(H2) | p(MPa) |
| I | 150 | 1/3 | 0.1 |
| II | 5 | ||
| III | 350 | 5 |
300��Cʱ�������������䣬���������ݻ�ѹ����ԭ����1/2����ƽ����ϵ������Ӱ����(����ĸ)�� ��
A��c(H2)���� B������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
C��CH3OH�����ʵ������� D������ƽ��ʱc(H2)/c(CH2OH)��С
����֪�ڳ��³�ѹ�£�
��2CH3OH(l)��3O2(g)=2CO2(g)��4H2O(g)DH=-1275.6 kJ��mol��1
��2CO(g)��O2(g)=2CO2(g) DH=-556.0 kJ��mol��1
��H2O(g)=H2O(l)DH=-44.0 kJ��mol��1
 д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ ��
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ ��
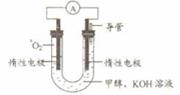
��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ�����������ͼ��ʾ�ĵ��װ�á�
�ٸõ�������ĵ缫��ӦΪ ��
�ڹ���һ��ʱ������Һ��pH��С���õ���ܷ�Ӧ�Ļ�ѧ����ʽΪ
��
���𰸡������� �ƣ� 1.35��10-3
��CD ʵ��II 150 1/3 ʵ��III 1/3
��CH3OH(l)+O2(g)![]() CO(g)+2H2O(g) DH= -447.8 kJ��mol��1
CO(g)+2H2O(g) DH= -447.8 kJ��mol��1
�ɢ�O2+2H2O+4e-=4OH- 2CH3OH+3O2+4KOH=2K2CO3+6H2O
������������С�������ݻ�������ѹǿ�������淴Ӧ���ʾ��ӿ졣��������ͼ��֪�¶����ߣ�CH4��ת���ʱ��˵���÷�Ӧ������ӦΪ���ȷ�Ӧ��
��100��ʱ��CH4��ת����Ϊ0.5������
CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
��ʼ��0.2mol 0.3mol 0 0
�仯��0.1mol 0.1mol 0.1mol 0.3mol
ƽ�⣺0.1mol 0.2mol 0.1mol 0.3mol
K=c(CO)��c(H2)3/[c(CH4)��c(H2O)]=0.01��0.033/(0.01��0.02)=1.35��10-3��
����Ȼ��ͬѧͨ�������Ʊ�������̽����������Ի�ѧƽ���Ӱ�죬̽����ǰ��ֻ���Ǹı�һ���������������������䣬��ʵ��II���¶���150�棬n(CO)/n(H2)=1/3��ͬ��ʵ��III��n(CO)/n(H2)ͬ������1/3��
���ڷ�ӦCO(g)+2H2(g)![]() CH3OH(g)�����������С�ķ�Ӧ���������С��������ѹǿ����Ӧ����������Ũ�Ⱦ��������淴Ӧ���ʾ��ӿ죬��ѧƽ��������Ӧ�����ƶ������Ϸ�����ѡ��C��D��ȷ��
CH3OH(g)�����������С�ķ�Ӧ���������С��������ѹǿ����Ӧ����������Ũ�Ⱦ��������淴Ӧ���ʾ��ӿ죬��ѧƽ��������Ӧ�����ƶ������Ϸ�����ѡ��C��D��ȷ��
�ȸ��ݸ�˹���ɵ�(�١���+�ۡ�4)/2��CH3OH(l)+O2(g)![]() CO(g)+2H2O(g) DH= -447.8 kJ��mol��1��
CO(g)+2H2O(g) DH= -447.8 kJ��mol��1��
�ɸ��������ԭ��ط�Ӧ���ܷ�ӦʽΪ2CH3OH+3O2+4KOH=2K2CO3+6H2O���ʵ�����Һ��pH��С��
�����㡿��ѧ��Ӧ�����뻯ѧƽ�� �������Һ


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
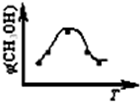 ��2012?����ģ�⣩��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϣ�
��2012?����ģ�⣩��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������˼״�����Ϊ21���͵�����ȼ�ϣ�| 3 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| V2 |
| a2 |
| V2 |
| a2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ʵ���� | T���棩 | n��CO��/n��H2�� | P��MPa�� | ||||
| i | 150 |
|
0.1 | ||||
| ii | 150 150 |
|
5 | ||||
| iii | 350 |
|
5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 | 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com