
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
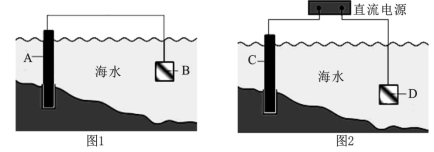
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择 (填字母序号)。
a.碳棒 b.锌板 c.铜板
该电化学保护方法的名称是 。
(2)图2中,钢闸门C为 极,用氯化钠溶液模拟海水进行实验,D为石墨块,总反应的离子方程式为 。
(3)有关上述实验,下列说法正确的是 。
A.溶液中Na+向D极移动
B.从D极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
(4)模拟工业上离子交换膜法制烧碱的方法,可用如图装置电解硫酸钾溶液来制取H2、O2、H2SO4和KOH。
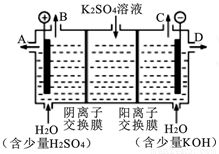
①该电解槽的阳极反应方程式为 。 此时通过阴离子交换膜的离子数 (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”) 导出。
③若采用CH4燃料电池(石墨为电极,KOH为电解质溶液)为电源,则该电池的负极电极方程式为 ,若B极产生标准状况下22.4 L气体,则理论上需要通入 mol CH4。
④电解过程中阴极区碱性明显增强,用平衡移动原理解释原因 。
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2015-2016学年福建省高二下学期期末化学试卷(解析版) 题型:选择题
有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。对此实验下述结论正确的是( )
A. Na2SO3已部分被空气中的氧气氧化
B. 加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4
C. 题中操作可证明Na2SO3溶液是否被氧化
D. 此实验不能确定Na2SO3是否部分被氧化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南师大附中高一下期末理综化学试卷(解析版) 题型:选择题
将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示。此电池工作时,下列叙述正确的是( )
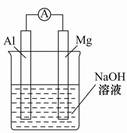
A.Mg比Al活泼,Mg失去电子被氧化成Mg2+
B.铝条表面虽有氧化膜,但可不必处理
C.该电池的内外电路中,电流均是由电子定向移动形成的
D.Al是电池负极,开始工作时溶液中会立即有白色沉淀析出
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高一下学期期末联考化学试卷(解析版) 题型:选择题
下列化学用语表述正确的是
A.原子核内有8个中子的碳原子:
B.NH4Cl的电子式: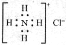
C.HClO的结构式:H- Cl - O
D.Ca2+的结构示意图: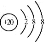
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高一下学期期末联考化学试卷(解析版) 题型:选择题
下列不属于取代反应的是
A.用日光照射甲烷与氯气的混合气体
B.乙烯通入溴水中
C.在FeBr3作催化剂的条件下,苯与液溴反应
D.乙醇与乙酸的酯化反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高二下学期期末联考化学试卷(解析版) 题型:选择题
25℃时,用0.100 mol/L NaOH溶液分别滴定20.00mL 0.100 mol/L 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是

A.II表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗V(NaOH)小于20mL
C.V(NaOH) =20.00mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH) =10.00mL时,醋酸溶液中:c(Na+)>c(CH3COO-)>c(H+ )>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省广安市邻水等高二下学期期末联考化学试卷(解析版) 题型:选择题
用相对分子质量为43的烷基取代甲苯苯环上的一个氢原子所得芳香烃产物的数目有
A. 3种 B. 4种 C. 5种 D. 6种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高一下期末化学试卷(解析版) 题型:选择题
如图是四种常见有机物分子的比例模型示意图。下列说法正确的是
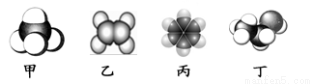
A.甲是甲烷,甲烷的二氯取代产物只有一种结构
B.乙是乙烯,乙烯可与溴水发生取代反应使溴水褪色
C.丙是苯,苯结构比较稳定,不能发生氧化反应
D.丁是乙酸,一定条件下乙酸能跟乙醇发生酯化反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
为了测定铁铜合金的组成,将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,将合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中H+的浓度为0.5mol•L-1,若反应前后溶液的体积变化忽略不计,则下列判断正确的是
A.上述反应中金属共失去电子0.1mol
B.合金中,铜的质量为2.8g
C.原硝酸的浓度:c(HNO3)=4.5mol•L-1
D.要使溶液中的金属离子完全沉淀,需加5mol•L-1的NaOH溶液60mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com