
| A. | HF、HCl、HBr、HI的熔点沸点依次升高 | |
| B. | HF、HCl、HBr、HI水溶液的酸性依次升高 | |
| C. | 乙醇易溶于水,是因为乙醇分子与水分子之间只存在范德华力 | |
| D. | 氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
分析 A、HF分子之间存在氢键,故熔点沸点相对较高;
B、根据氢离子的电离程度判断酸性的强弱;
C、乙醇分子与水分子之间存在氢键和范德华力;
D、Cl元素的化合价越高,对应的氧化物的水化物的酸性越强.
解答 解:A、HF分子之间存在氢键,故熔点沸点相对较高,故熔点沸点的大小关系为HF>HI>HBr>HCl,故A错误;
B、在物质中H-X之间的化学键键长增大,氢离子的电离程度逐渐增大,酸性增强,故B正确;
C、乙醇分子与水分子之间除了存在范德华力,还存在氢键,故C错误;
D、Cl元素的化合价越高,对应的氧化物的水化物的酸性越强,应为HClO<HClO2<HClO3<HClO4,故D错误.
故选B.
点评 本题考查氢键的形成与性质,题目难度不大,注意氢键与分子间作用力、化学键的区别,易错点为氢键对物质性质的影响.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
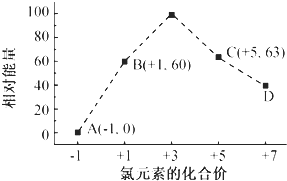 元素周期表的用途广泛.
元素周期表的用途广泛.| 离子半径 | 非金属性 | 酸性 | 沸点 |
| K+<S2- | N<O | 硫酸<高氯酸 | HF>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 物质B的转化率增大 | B. | 平衡向正反应方向移动 | ||
| C. | 物质A的体积分数增大 | D. | a+b<m+n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在某溶液中滴加AgNO3溶液,若产生白色沉淀,说明该溶液中有Cl- | |
| B. | 在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- | |
| C. | 在某溶液中先滴加AgNO3溶液,产生色沉淀,再滴加盐酸,沉淀不消失,说明溶液中Cl- | |
| D. | 某溶中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12O的醇能够被催化氧化生成醛,该醇的同分异构体有4种 | |
| B. | 将苯、溴水和铁屑混合制溴苯 | |
| C. | (C6H10O5)n可以是淀粉或纤维素,二者均属于多糖,且互为同分异构体 | |
| D. | 若不考虑立体异构,分子式为C4H8O2且为酯的同分异构体有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入催化剂能加快反应速率 | |
| B. | 增大压强能减慢反应速率 | |
| C. | 达到平衡时,反应速率:v(正)=v(逆)=0 | |
| D. | 达到平衡时,N2和H2能100%转化为NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
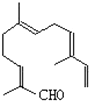
| A. | 有机物X的分子式为Cl2H15O | |
| B. | X分子不能使酸性高锰酸钾溶液褪色 | |
| C. | X分子中一定在同一个平面内的碳原子最多6个 | |
| D. | 在Ni作催化剂的条件下,1molX最多能与4molH2加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com