
【题目】下列有关有机物的说法中
①结构片段为…… ……的高聚物,其单体是甲醛和苯酚
……的高聚物,其单体是甲醛和苯酚
②标准状况下,22.4LHF所含电子数约为10NA
③甲醇通常是一种有毒的气体,分子中只含极性键
④苯酚和碳酸钠溶液的反应:![]()
⑤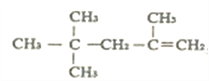 的名称为:2,4,4,-三甲基-1-戊烯
的名称为:2,4,4,-三甲基-1-戊烯
⑥3-甲基-1-丁烯中的所有碳原子不可能处于同一平面
⑦等物质的量的苯与苯甲酸完全燃烧消耗氧气的量不相等
其中正确的有 个。
A. 4 B. 5 C. 6 D. 7
【答案】A
【解析】①苯酚和甲醛发生缩聚反应得到酚醛树酯,结构片段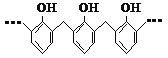 ,故①正确;②标准状况下,HF为液体,不能根据气体的摩尔体积计算其物质的量为,故②错误;③甲醇分子中只含极性键,是一种有毒性的液体,故③错误;
,故①正确;②标准状况下,HF为液体,不能根据气体的摩尔体积计算其物质的量为,故②错误;③甲醇分子中只含极性键,是一种有毒性的液体,故③错误;
④苯酚的酸性比HCO3-强,苯酚和碳酸钠溶液的反应方程式为![]() ,故④正确;⑤有机物
,故④正确;⑤有机物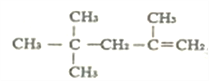 的名称为2,4,4-三甲基-1-戊烯,故⑤正确;⑥碳碳双键只能确保与双键相连的碳原子在同一平面上,则3-甲基-1-丁烯中的所有碳原子不可能处于同一平面上,故⑥正确;⑦x+
的名称为2,4,4-三甲基-1-戊烯,故⑤正确;⑥碳碳双键只能确保与双键相连的碳原子在同一平面上,则3-甲基-1-丁烯中的所有碳原子不可能处于同一平面上,故⑥正确;⑦x+![]() =6+
=6+![]() =7.5,即1mol苯消耗氧气7.5mol,苯甲酸的x+
=7.5,即1mol苯消耗氧气7.5mol,苯甲酸的x+![]() -
-![]() =7+
=7+![]() -1=7.5,即1mol苯甲酸消耗氧气7.5mol,所以等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等,故⑦错误;共4个正确,答案为A。
-1=7.5,即1mol苯甲酸消耗氧气7.5mol,所以等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等,故⑦错误;共4个正确,答案为A。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E五种原子序数依次增加的短周期元素,其中A的最低负价和最高正价代数和为零,且A2常温下为气态,B与其他元素形成的化合物种类最多,C与E可形成EC2和EC3两种物质,D是短周期最活泼的金属元素,用化学用语回答下列问题:
(1)D离子结构示意图________,用电子式表示BC2形成过程____________;
(2)A与C形成含18个电子的化合物的电子式是_________________;
(3)C与D形成的一种化合物颜色为淡黄色,其阴阳离子个数比为______,电子式为________,所含化学键为___________;
(4)B、E两元素得电子能力B____E(填“>”或“<”),试写出证明该结论的一个化学方程式__________;
(5)工业上常用足量氨水吸收尾气中的EC2,离子方程式为_______,检验其中阳离子的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的 X 置于某 10 L 容积恒定的真空容器中(假设固体试样体积忽略不计),在恒定温度下使其达到分解平衡:X(s)![]() 2Y(g)+Z(g),实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是( )
2Y(g)+Z(g),实验测得不同温度下的分解平衡常数列于下表,下列说法中不正确的是( )
温度( oC) | 15.0 | 25.0 | 30.0 | 35.0 |
K/(×10-8 mol3·L-3) | 0.205 | 1.64 | 4.68 | 10.8 |
A.若Z的体积分数不再随时间变化时表示反应达平衡状态
B.35 oC时,达平衡时,X分解了 0.03 mol
C.该反应在高温下可能自发
D.若在恒温下,压缩容器体积,再次达平衡后,n(X)比原平衡大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应在__________min时达到平衡状态;
(2)该反应的化学方程式为_________________________________________________。
(3)反应开始至2 min,气体Z的反应速率为______________________________。
(4)若X、Y、Z均为气体,反应达到平衡时压强是开始时的____________倍;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于植物细胞中元素的叙述,错误的是
A. 番茄和水稻根系吸Si元素的量有差异
B. 细胞中含量最多的四种元素是C、O、H和N
C. 植物根系通过主动运输吸收无机离子需要ATP
D. 细胞膜的选择透过性与膜蛋白有关,与脂质无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】查看葡萄酒标签上的成分信息时,常发现其成分中含有少量SO2 。下列关于SO2说法正确的是
A. SO2属于非法添加剂,不该添加到葡萄酒中
B. SO2具有还原性,不能用浓硫酸干燥
C. SO2具有还原性,少量的SO2可防止葡萄酒氧化变质
D. SO2可以使酸性KMnO4溶液褪色,体现了它的漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年10月17日7点30分,神舟十一号载人飞船发射升空。制造航天飞船的主要材料是铝,工业上制铝时用冰晶石(Na3AlF6)做助熔剂,冰晶石制备流程有如下两种:
方案一:以纯碱和萤石(CaF2)为主要原料
![]()
方案二:以碳酸氢铵和六氟合硅酸为主要原料

(1)方案一中B可作为建筑材料,化合物A 是________,写出由C制备冰晶石的化学方程式____________________________。
(2)方案二中反应1产生的气体是_____________,反应2后滤液中主要成分的用途_________。
(3)方案二中反应2化学方程式________________________。
(4)工业电解制铝的阴极反应式为_________________,以石墨为电极维持电流180千安电解5小时生成铝270千克,则电流效率η(η=实际产量/理论产量)为_______。(法拉第常数F = 96500 C·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作错误的是( )
A. 滴定管经蒸馏水洗净后,即可注入标准液进行滴定
B. 玻璃导管蘸水后,边旋转边向橡皮管中插入
C. 滴定用锥形瓶经蒸馏水洗净后,不须用标准液润洗
D. 用玻璃棒蘸取待测液滴到pH试纸上,然后跟标准比色卡相对照,读出pH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com