
| A. | 加入Al能放出H2的溶液中:Fe2+、Al3+、NO3-、Cl- | |
| B. | pH=13的溶液中:Na+、CO32-、K+、HCO3- | |
| C. | 在无色溶液中:Cu2+、Ca2+、SO42-、Cl- | |
| D. | 加入Mg能放出H2的溶液中:Mg2+、Cl-、K+、SO42- |
分析 A.加入Al能放出H2的溶液中存在大量氢离子或氢氧根离子,亚铁离子、铝离子与氢氧根离子反应,酸性条件下硝酸根离子能够氧化亚铁离子;
B.pH=13的溶液中存在电离氢氧根离子,碳酸氢根离子与氢氧根离子反应;
C.铜离子与无色离子,钙离子与硫酸根离子反应生成微溶物硫酸钙;
D.加入Mg能放出H2的溶液中存在电离氢离子,四种离子之间不反应,都不与氢离子反应.
解答 解:A.加入Al能放出H2的溶液为酸性或碱性溶液,Fe2+、Al3+与碱性溶液中的氢氧根离子反应,酸性条件下Fe2+、NO3-之间发生氧化还原反应,在溶液中一定不能大量共存,故A错误;
B.pH=13的溶液为碱性溶液,溶液中存在电离氢氧根离子,HCO3-与氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.Cu2+为有色离子,且大量的Ca2+、SO42-之间反应生成硫酸钙沉淀,在溶液中一定不能大量共存,故C错误;
D.加入Mg能放出H2的溶液为酸性溶液,溶液中存在电离氢离子,Mg2+、Cl-、K+、SO42-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;是“可能”共存,还是“一定”共存等.


科目:高中化学 来源: 题型:选择题
| A. | 逆反应速率增大更大,平衡向逆反应方向移动 | |
| B. | 正反应速率增大更大,平衡向正反应方向移动 | |
| C. | 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 | |
| D. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
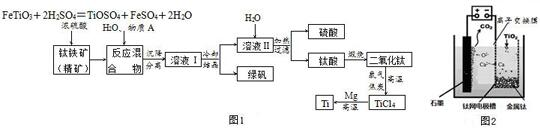
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
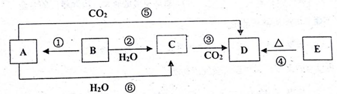
| 现象 | 单质B的相关性质(填序号) | 相关的化学方程式 | |
| Ⅰ | 单质B浮在水面上 | ||
| Ⅱ | 熔成一个小球 | ||
| Ⅲ | 四处游动,发出嘶嘶的声音 | ||
| Ⅳ | 滴入酚酞试剂,溶液变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
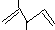 名称:2,3-二甲基-1,5-戊二烯 ②乙烯的实验式;CH2
名称:2,3-二甲基-1,5-戊二烯 ②乙烯的实验式;CH2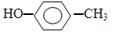
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
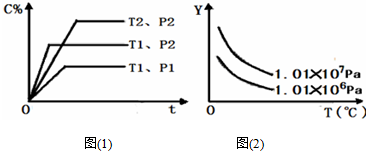
| A. | 反应物A的百分含量 | B. | 反应物B的平衡转化率 | ||
| C. | 平衡混合气的密度 | D. | 平衡混合气的总物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
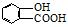 ⑤聚乙烯⑥
⑤聚乙烯⑥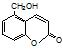 ,⑦丁子香酚
,⑦丁子香酚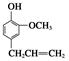
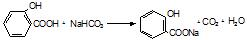 .
.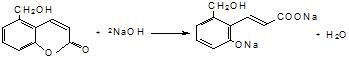 .
.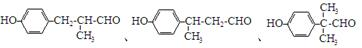 等.
等.查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第三次月考化学卷(解析版) 题型:选择题
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是
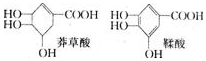
A.等物质的量的两种物质跟足量的NaOH反应,消耗NaOH的量相等
B.完全燃烧等物质的量的两种物质生成二氧化碳和水的量分别相等
C.一定条件下,两种物质都能发生酯化反应和氧化反应
D.鞣酸分子中,可能在同一平面上的原子最多有14个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com