
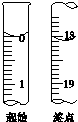
 Na2SO3���ױ�������Na2SO4�����ʣ�ij��ѧ��ȤС��Ϊ�˲ⶨʵ���Ҵ�ŵ�Na2SO3�Ĵ��ȣ����費���������ʣ�����������ʵ�飮
Na2SO3���ױ�������Na2SO4�����ʣ�ij��ѧ��ȤС��Ϊ�˲ⶨʵ���Ҵ�ŵ�Na2SO3�Ĵ��ȣ����費���������ʣ�����������ʵ�飮| 250ml |
| 25ml |
| V��10-3mol��126g/mol |
| mg |
| 12.6V |
| m |
| 12.6V |
| m |


 ���¿쳵����������ϵ�д�
���¿쳵����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����H��0����S��0 |
| B����H��0����S��0 |
| C����H��0����S��0 |
| D����H��0����S��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
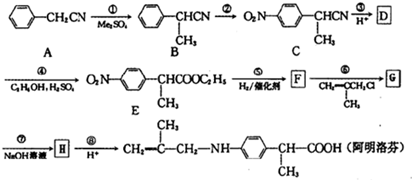
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
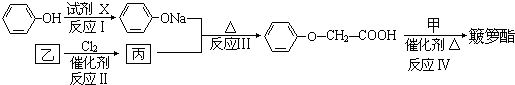
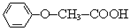 ������������Ӧ�IJ��
������������Ӧ�IJ��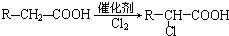 ��R-ONa
��R-ONa| Cl-R�� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol?L-1 |
| B��0.2 mol?L-1 |
| C��0.4 mol?L-1 |
| D��0.8 mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �˴Ź���������
�˴Ź����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ᡢ��ˮ�����ᱵ������������ʡ� |
| B��ͭ�Ͻ����Ͻ𡢸��������ڽ������� |
| C�������͡�ֲ���͡������;������������ |
| D��ϡ������ϡ���ᡢ�轺�����ڽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij��Һ�У�Ca2+��H+��Cl-��HSO3- |
| B����ʹPH��ֽ�ʺ�ɫ����Һ��Na+��NH4+��Fe2+��NO3- |
| C��Na2CO3��Һ��K+��Fe3+��SO42-��NO3- |
| D��Kw/c��H+��=0.1mol/L����Һ��Na+��K+��S2-��NO3- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com