
【题目】下图表示氮及其化合物在一定条件下的转化关系:

(1)反应I:N2(g)+3H2(g)![]() 2NH3(g) ΔH=–92 kJmol-1
2NH3(g) ΔH=–92 kJmol-1
下左图是反应I中平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是________(填“温度”或“压强”)。

(2)①反应II的化学方程式是_________________________。
②反应II其中一步反应为2NH3(g)+3Cl2(g) =N2(g) +6HCl(g) ΔH=–462 kJmol-1
已知:N2(g)![]() 2N(g) Cl2(g)
2N(g) Cl2(g)![]() 2Cl(g)
2Cl(g)
断开1 mol H–N键与断开1 mol H–Cl键所需能量相差约为________kJ。
(3)(3)反应III是利用右上图所示装置电解制备NCl3(氯的化合价为+1),其原理是:NH4Cl+2HCl![]() NCl3+3H2↑。
NCl3+3H2↑。
①b接电源的_______极(填“正”或“负”)。② 阳极反应式是___________________。
(4)反应III得到的NCl3可以和NaClO2制备 ClO2,同时生成NH3,该反应的离子方程式是________。
【答案】 压强 8NH3+3Cl2=N2+6NH4Cl 41 负 3Cl--6e-+NH4+=NCl3+4H+ NCl3+6ClO2-+3H2O=6ClO2+NH3+3C1-+3OH-
【解析】(1)由图像得出:随着X的增大,氨气的体积分数应该增大。升高温度,平衡向逆反应方向移动,氨气的体积分数应该减小,所以X不可能代表温度。增大压强,平衡向正反应方向移动,氨气的体积分数增大,所以X应该代表压强。
(2)①根据转化关系可以判断,反应物为![]() 和
和![]() ,生成物为
,生成物为![]() 和
和![]() ,然后根据得失电子守恒和原子守恒配平,化学方程式为
,然后根据得失电子守恒和原子守恒配平,化学方程式为![]() 。
。
②化学反应的过程是旧化学键断裂(吸收能量)和新化学键形成(放出能量)的过程,设断开1 mol H–N键吸收a kJ能量,断开1 mol H–Cl键吸收b kJ能量,根据化学反应2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) ΔH=–462 kJmol-1,得到6×a+3×243-945-6×b=-462,得![]() ,所以断开1 mol H–N键与断开1 mol H–Cl键所需能量相差约为41kJ。
,所以断开1 mol H–N键与断开1 mol H–Cl键所需能量相差约为41kJ。
(3)①b电极的反应为H+得电子生成氢气,发生还原反应,所以b电极为阴极,连接电源的负极。
②阳极反应物为NH4Cl,生成物为NCl3 ,题目中给出氯的化合价为+1价,所以氯失去电子,化合价升高,氮、氢不变价,然后根据电荷守恒配平方程式,则阳极反应式是![]()
(4)根据题意,![]() 可以和
可以和![]() 制备
制备![]() ,同时生成
,同时生成![]() ,反应物为
,反应物为![]() ,生成物为
,生成物为![]() ,根据化合价升降相等、电荷守恒和原子守恒配平,该反应的离子方程式是NCl3+6ClO2-+3H2O=6ClO2+NH3↑+3C1-+3OH- 。
,根据化合价升降相等、电荷守恒和原子守恒配平,该反应的离子方程式是NCl3+6ClO2-+3H2O=6ClO2+NH3↑+3C1-+3OH- 。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】白磷在氧气中燃烧的反应为:P4 + 5O2 = P4O10。已知下列化学键的键能分别为:P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据,下列推断正确的是

A.6a+5d < 4c + 10b
B.△H = (4c+12b-6a-5d) kJ·mol-1
C.6a+5d > 4c + 12b
D.△H = (6a+5d-4c-12b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以原油为原料生成聚烯烃的步骤如下:
![]()
试回答:
(1)含有10个氢原子的烷烃的分子式为_____________;
(2)C4~C10的烃类混合物含有______________(填“等于”、“少于”或“多于”)7种不同的物质。
(3)写出由丙烯生成聚丙烯的化学方程式________________________________________,属于__________类型反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,能够成立的是( )
CO(g)+H2(g)在一密闭容器中进行,则下列说法或结论中,能够成立的是( )
A. 其他条件不变仅将容器的体积缩小一半,反应速率减小
B. 反应达平衡状态时:v正(CO)=v逆(H2O)
C. 保持体积不变,充入少量He使体系压强增大,反应速率一定增大
D. 其他条件不变,适当增加C(s)的质量会使反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) ![]() 3Z(g) ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
3Z(g) ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
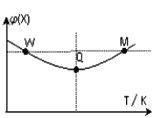
A. Q点时,Y的转化率最大
B. W点X的正反应速率等于M点X的正反应速率
C. 升高温度,平衡常数增大
D. 温度一定,平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( ) 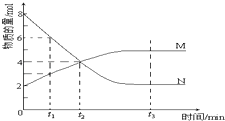
A.反应的化学方程式:N2M
B.t2时,正、逆反应速率相等,达到平衡
C.t2时,正反应速率大于逆反应速率
D.恒温恒容下,当N的化学反应速率是M的两倍时,则证明达到了化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:15P、33As位于同一主族,下列关系正确的是
A. 原子半径:As>Cl>P B. 热稳定性:HCl>PH3>AsH3
C. 非金属性:Cl>As>S D. 酸性:H3AsO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A.该反应的化学方程式为3B+2D 6A+4C
B.反应进行到1 s时,v(A)=3v(D)
C.反应进行到6 s时,B的平均反应速率为0.1mol/(Ls)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com