
| A、1L 1mol/L氯化铜溶液中含有NA个Cu2+ | B、标准状况下,22.4L O2参加任何化学反应转移的电子数都是4NA | C、1mol Zn与足量稀HNO3反应,转移2NA个电子 | D、1mol H3O+所含电子数为8NA |


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
| A、18g金刚石中,碳碳共价键数为3NA | B、在H2O2+Cl2→2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 | C、常温常压时S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA | D、一定温度下,1L 0.50mol?L-1 NH4Cl溶液与2L 0.25mol?L-1 NH4Cl溶液中NH4+的物质的量均小于0.5NA,且前者更少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,1mol甲基(14C1H3-)所含的中子数和电子数分别为8NA、9NA | B、标准状况下,22.4L 己烷中共价键数目为19NA | C、标准状况下,2.24L Cl2全部被NaOH溶液吸收,转移的电子数目为0.2NA | D、在高温、高压、催化剂的条件下,28gN2和6gH2充分反应,生成NH3的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、45gHCH0与CH3COOH混合物含氢原子数为3NA | B、常温常压下,54g重水(D20)含水分子数为3NA | C、标准状况下,11.2L苯含有C-H键数目为3NA | D、反应KIO3+6HI=3I2+KI+3H20,每生成1.5mol I2转移电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某温度下,1 L pH=8的纯水中含OH-为10-8NA | B、14 g分子通式为CnH2n的链烃中含有的C=C键数目为NA | C、标准状况下,22.4 L Cl2与足量Fe反应,转移的电子数为3NA | D、常温下,1 L 0.1 mol?L-1 CH3COONa溶液中含有的Na+和CH3COO-总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8g Na2O2中所含阴离子的数目为0.2NA | B、标准状况下,2.24L 18O2中所含中子的数目为2NA | C、物质的量浓度为1mol/L的NaOH溶液中含Na+数目为NA | D、1mol Fe与一定量HNO3恰好完全反应时,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用盐析法分离NaCl溶液和淀粉胶体 | B、天然油脂的分子中含有酯基,属于酯类 | C、T℃时,1L pH=6的纯水中,含有的OH-数目为l×10-6NA | D、12.0 gNaHSO4固体中含有的阳离子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、28g CO和16g O2所含的氧原子数都为NA | B、100mL 0.1 mol?L-1 AlCl3溶液中Al3+总数为0.01NA | C、标准状况下,22.4L CO2和O2的混合气体含有的分子总数为NA | D、5.6g Fe与足量Cl2反应时转移电子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
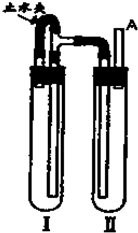 白色的Fe(OH)2沉淀在空气中极易被氧化.利用如图装置可以制得白色的Fe(OH)2沉淀,并能在较长时间内保持白色.实验中可选用的试剂有:NaOH溶液、铁屑、稀H2SO4.
白色的Fe(OH)2沉淀在空气中极易被氧化.利用如图装置可以制得白色的Fe(OH)2沉淀,并能在较长时间内保持白色.实验中可选用的试剂有:NaOH溶液、铁屑、稀H2SO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com