

| ||
| cu |
| △ |
| cu |
| △ |


科目:高中化学 来源: 题型:
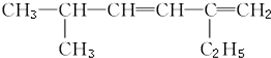
| A、2-甲基-5-乙基-3,5己二烯 |
| B、2-乙基-1,3-己二烯 |
| C、6-甲基-3,4-庚二烯 |
| D、5-甲基-2-乙基-1,3-己二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:


 )的一条路线如下:
)的一条路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (其中I、Ⅱ为未知部分的结构)为推测X的分子结构,进行如图的转化:
(其中I、Ⅱ为未知部分的结构)为推测X的分子结构,进行如图的转化:
查看答案和解析>>
科目:高中化学 来源: 题型:
 以下框图中的字母代表1-20号元素形成的常见单质及化合物,这些物质之间转化关系如图所示:其中A、B、C为单质,其余为化合物,J常温下呈液态,B在A中燃烧产生苍白色火焰,实验室常用①反应制取气体E,反应②为侯德榜制碱法的主要反应原理,L为常见的干燥剂.
以下框图中的字母代表1-20号元素形成的常见单质及化合物,这些物质之间转化关系如图所示:其中A、B、C为单质,其余为化合物,J常温下呈液态,B在A中燃烧产生苍白色火焰,实验室常用①反应制取气体E,反应②为侯德榜制碱法的主要反应原理,L为常见的干燥剂.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中肼作还原剂 |
| B、此情况下,液态肼燃烧生成1molN2时放出的热量为641.6kJ |
| C、肼(N2H4)分子中只存在极性共价键 |
| D、该反应的反应物总能量高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、该反应是吸热反应 |
| B、加入催化剂后,反应加快, |
| C、反应物的总键能小于生成物的总键能 |
| D、反应达到平衡时,升高温度,A的转化率增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com