
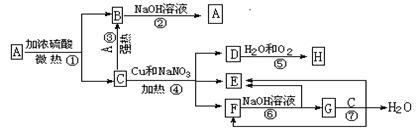
科目:高中化学 来源:不详 题型:填空题
| 火烧孔雀石炼铜 | 湿法炼铜 | 铝热法炼铬 | 从光卤石中炼镁 |
| | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
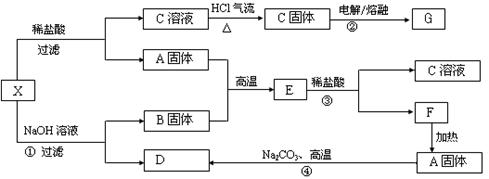 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
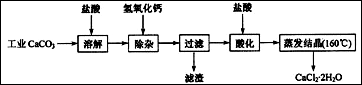
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含金属元素的离子一定是阳离子 |
| B.向新制的FeCl2溶液中滴加NaOH溶液,有红褐色沉淀生成 |
| C.氯水和过氧化钠都具有漂白作用,其漂白原理相似 |
| D.如果将过量的二氧化锰与20mL、12mol?L-1的盐酸混合加热,充分反应生成氯气的物质的量一定为0.06mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com