
25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. 0.1mol/L NaHSO4溶液中:K+、AlO2-、Cl-、CH3COO-
B. 0.1mol/L NaHCO3溶液中:Al3+、Ca2+、SO42-、NO3-
C. 0.1mol/L FeCl3溶液中: NH4+、NO3-、Na+、SO42-
D. 0.1mol/L H2O2溶液中:Na+、K+、SO32-、Cl-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年河北省高二下学期3月月考化学试卷(解析版) 题型:选择题
某酯完全燃烧生成等摩的CO2和H2O,把该酯水解可得羧酸 B和醇C,把醇C氧化可得羧酸D,且B与D互为同分异构体,则此酯为 ( )
A.CH3CH2COOCH(CH3)2
B.CH3CH2COOCH2CH2CH=CH2
C.(CH3)2CHCOOCH2CH(CH3)2
D.CH3CH2CH2COOCH2CH(CH3)2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期期中考试化学试卷(解析版) 题型:选择题
高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是

A. 该反应过程中的能量变化如图所示
B. 该反应条件下,Al的还原性弱于Fe
C. 1molFe3O4参与反应转移8×6.02×1023个电子
D. 实验室进行该反应时常加入KClO3作催化剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期期中考试化学试卷(解析版) 题型:选择题
医学研究证明,用放射性 治疗肿瘤可收到一定疗效。下到有关
治疗肿瘤可收到一定疗效。下到有关 叙述正确的是
叙述正确的是
A.  碘的一种同素异形体 B.
碘的一种同素异形体 B.  是一种新发现的元素
是一种新发现的元素
C.  位于元素周期表中第四周期第VIIA族 D.
位于元素周期表中第四周期第VIIA族 D.  核内的中子数与核外电子数之差为29
核内的中子数与核外电子数之差为29
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(一)化学试卷(解析版) 题型:实验题
过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备

(1)步骤①加入氨水的目的是_______。小火煮沸的作用是使沉淀颗粒长大,有利于____。
(2)下图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。

a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备

(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈____性(填“酸”、“碱”或“中”)。将溶液煮沸,趁热过滤。将溶液煮沸的作用是___________。
(4)步骤③中反应的化学方程式为________,该反应需要在冰浴下进行,原因是_________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_______。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是______,产品的缺点是_______。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(一)化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 在海轮船壳上镶入锌块保护海轮,利用的是牺牲阳极的阴极保护法
B. KNO3溶液和CH3OONH4溶液均显中性.两溶液中水的电离程度相等
C. 若1 molNa2O2与足量水反应产生O2,理论上转移的电子数约为2×6.02×1023
D. 用pH 均为2 的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
查看答案和解析>>
科目:高中化学 来源:2017届北京市朝阳区高三第一次(3月)综合练习理综化学试卷(解析版) 题型:填空题
将CH4、CO2催化重整为可用的化学品,对缓解能源危机、改善环境意义重大。

(l)以Fe(OH)3为脱硫剂,通过复分解反应吸收H2S,产物是H2O和___________。
(2)过程A主要涉及以下反应:
i. CH4(g)+CO2(g) 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
ii. CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ/mol
CO2(g)+H2(g) △H=-41kJ/mol
①反应i的化学平衡常数K随温度的变化关系是____。
②分析反应iixt反应i中CO2转化率可能的影响并说明理由:____(写出一种即可)。
(3)某科研团队利用Ni、CaO、Fe3O4三种催化剂在850℃下“超干重整”CH4和CO2;
过程I.通入CO2和CH4,所得CO被吸收,H2O被分离出体系,如下面左图所示。
过程Ⅱ.H2O被分离后,向该装置中再通入He气,使催化剂再生并获得CO,如下面右图所示。

①CH4和CO2重整为CO、H2O的热化学方程式是____________。
②结合反应方程式简述Fe3O4的催化作用:___________。
③CaO对Fe3O4是否起到催化作用至关重要,实验研究结果如下表:
编号 | 催化剂 | 是否添加CaO | 还原产物 |
1 | Fe3O4 | 添加 | 有Fe |
2 | Fe3O4 | 不添加 | 无Fe |
运用有关化学原理解释实验结果:____。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一下学期第一次月考(3月)化学试卷(解析版) 题型:选择题
短周期 元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是
元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是
A.原子半径:A<B<C
B.三种元素的最高价氧化物对应水化物均可由化合反应得到
C.A的氢化物稳定性大于C的氢化物稳定性
D.B 和A的最高价氧化物可发生置换反应
查看答案和解析>>
科目:高中化学 来源:2017届全国新课程高考仿真信息理综(一)化学试卷(解析版) 题型:实验题
席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:

已知以下信息:
①
②1molB经上述反应可生成2molC,且C不能发生银镜反应。
③D属于单取代芳香烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的氢。
⑤
回答下列问题:
(1)由A生成B的化学方程式为______________,反应类型为________。
(2)D的化学名称是________,由D生成E的化学方程式为:_______________。
(3)G的结构简式为__________________。
(4)F的同分异构体中含有苯环的有多种(不考虑立体异构)。其中核磁共振氢谱中有4组峰,且面积比为6:2:2:1的是____________。(写出其中的一种的结构简式)。
(5)由苯和化合物C经如下步骤可合成N-异丙基苯胺。
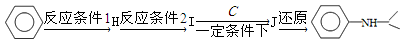
反应条件1所选择的试剂为_______;反应条件2所选择的试剂为________;I的结构简式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com