
下列说法正确的是
A. 原子的L层上的电子数为奇数的元素一定是主族元素
B. 同一周期的ⅡA族和ⅢA族元素的原子序数之差一定为1
C. 相邻两个周期的同一主族元素的原子序数之差等于上一周期所含元素种类
D. 主族序数等于周期序数的元素一定为金属元素
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:高中化学 来源: 题型:
影片《阿凡达》中出现了一艘开往潘多拉星球的宇宙飞船。下图是元素周期表中的一部分,表中所列字母分别表示一种元素(选项中的物质都是由下图中的元素组成)。根据以上信息,下列说法正确的是( )
A.e和f组成的化合物可吸收宇航员在宇宙飞船活动舱内产生的由d和f组成的气体
B.活动舱内还要营造一种适合宇航员生存的人工生态环境,即充入a和f的常见单质
C.c和f以原子个数之比为1∶1组成的化合物可用作宇航员所需f单质的来源
D.若潘多拉星球上存在b原子, 但比地球上此元素原子少一个质子

查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
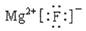
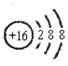
A.硫离子的结构示意图: B.氟化镁的电子式:
C.甘氨酸的结构式:C2H5O2N
D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH)22-
查看答案和解析>>
科目:高中化学 来源: 题型:
化学和环境保护、食品营养、材料应用等密切相关。
(1)(3分)防治环境污染、改善生态环境已成为全人类的共识。
①下列各项中,完成空气质量报告时不需要监测的是 (填字母)。
a.可吸入颗粒物的浓度 b.二氧化氮的浓度
c.二氧化碳的浓度
②下列做法中不利于改善环境质量的是 (填字母)。
a.将废旧电池进行深埋处理 b.充分利用太阳能等清洁能源
c.给汽车加装尾气催化净化装置
③工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是 (填字母)。
a.沉淀法 b.中和法 c.氧化还原法
(2)(5分)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①人体需要的营养素主要有糖类、 、蛋白质、无机盐、维生素和水。在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是 。
②下列物质中,具有解热镇痛疗效的是 (填字母)。
a.氨基酸 b.阿斯匹林 c.青霉素
③有些药片常用淀粉作为黏合剂,淀粉进入人体后在人体内酶的催化作用下逐步水解,最终转化为 (填物质的名称)。维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和 试剂共同完成。
(3)(7分)材料是人类社会发展的物质基础,材料科学的发展离不开化学。
①陶瓷、水泥和普通玻璃都是生活中最常见的材料,它们属于 (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
制造普通玻璃时,需要的主要原料有纯碱、石灰石和 (填化学式)。
②钢铁制品在潮湿的空气中发生 (填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因。硬铝(一种铝合金)是制造飞机和宇宙飞船的理想材料,和纯铝相比,硬铝的强度 (填“低”、“高”或“无法确定”),具有较强的抗腐蚀能力。
③在尼龙、棉花、涤纶这三种物质中,属于天然纤维的是 。橡胶是制造轮胎的重要原料,天然橡胶通过 (填“硫化”、“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。“白色污染”已成为当今社会的一大公害,“白色污染”主要是 (填“废塑料制品”、“废橡胶制品”或“生活垃圾”)造成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中性质的变化规律排列正确的是
A.微粒半径:Al3 + >Mg2 + >Na + >F -
B.稳定性:HI>HBr>HCl>HF
C.酸性:HClO4>H2SO4>H3PO4>H4SiO4
D.碱性:Ca(OH)2>KOH>Mg(OH)2>Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能作为实验判断依据的是
A.钠和镁分别与冷水反应,判断钠和镁的金属活动性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱
C.硫酸和硅酸钠溶液反应出白色沉淀,判断硫与硅的非金属活动性强弱
D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
如表是ⅥA族部分元素的相关性质。
| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请回答下列问题:
(1)硒的熔点范围可能是 。
(2)碲的化合价可能有 。
(3)硫、硒最高价氧化物对应水化物的酸性强弱顺序是
(填化学式)。
(4)氢硒酸有较强的________(填“氧化性”或“还原性”),因此放在空气中易变质,其可能
发生反应的化学方程式为 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式。
Al2Te3+( )===2Al(OH)3↓+____H2Te↑
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
| 原子或分子相关信息 | 单质及其化合物相关信息 | |
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的1/2 | Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W在周期表的位置为 ,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为 。
(2)X的简单阴离子的结构示意图为 ,X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为 。
(3)Z的氧化物在通讯领域用来作 ,工业上制备Z的单质的化学反应方程式为 。
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它用来制造半导体晶体管,最新研究表明:有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应但在有H2O2 存在时可与NaOH 溶液反应生成锗酸盐,其方程式为 。
(4)在50 mL l mol·L-1的YX3溶液中逐滴加入0.5 mol·L-1的NaOH溶液,得到1.56 g沉淀,则加入NaOH溶液的体积可能 种情况(填一或二)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com