
| A�� | ������Ӧ�����û���Ӧ | B�� | ��Ӧ���Ƿ��ȷ�Ӧ | ||
| C�� | ����������Ӧ�ǿ��淴Ӧ | D�� | ������Ӧ����������ԭ��Ӧ |
���� A���û���Ӧ��һ�ֵ��ʺ�һ�ֻ����ﷴӦ������һ�ֵ��ʺͻ�����ķ�Ӧ��
B����Ӧ����Q��0��֤���÷�ӦΪ���ȷ�Ӧ��
C�����淴Ӧ����ͬһ������ͬʱ���еķ�Ӧ��
D����Ӧ������ Ԫ�ػ��ϼ۱仯Ϊ������ԭ��Ӧ��
��� �⣺A��������Ӧ����һ�ֵ��ʺ�һ�ֻ����ﷴӦ������һ�ֵ��ʺͻ�����ķ�Ӧ�������û���Ӧ�����A��ȷ��
B����Ӧ����Q��0��֤����Ӧ��Ϊ���ȷ�Ӧ����B��ȷ��
C��������Ӧ�ķ�Ӧ������ͬ�����ܳ�Ϊ���淴Ӧ����C����
D����Ӧ������Ԫ�ػ��ϼ۾��б仯�����Զ���������ԭ��Ӧ����D��ȷ��
��ѡC��
���� ���⿼����������ԭ��Ӧ����Ŀ�ѶȲ����漰���淴Ӧ����Ӧ���ͼ�������ԭ��Ӧ���жϣ�ע�������û���Ӧ��������ԭ��Ӧ�����淴Ӧ�ĸ���жϷ�����������ػ���֪ʶ�Ŀ��飬������ѧ�������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHSO4��Һ | B�� | NH4Cl��Һ | C�� | Al��NO3��3��Һ | D�� | NaCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2 | B�� | 3��1 | C�� | 1��3 | D�� | 2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڡ��ۻ�� | B�� | �ڡ��ۻ�� | C�� | �١��ۻ�� | D�� | �١��ۻ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
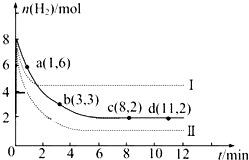 ��ҵ�ϡ��̶���������CO2����Ч�ؼ��ᡰ���ҡ�ЧӦ������CO2����ȼ�ϼ״���
��ҵ�ϡ��̶���������CO2����Ч�ؼ��ᡰ���ҡ�ЧӦ������CO2����ȼ�ϼ״����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� | 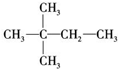 | D�� | 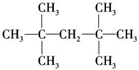 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com