
(10分)某化学课外活动小组将氯化钠固体中混有的硫酸钠、碳酸氢铵杂质除去并得到氯化钠溶液,设计了如下方案:

(1)操作①的目的是: ;
(2)操作②是否可改为加硝酸钡溶液?为什么? ;
(3)进行操作②后,如何判断SO42-已除尽,方法是: ;
(4)在操作③中为什么不在加Na2CO3溶液之前先过滤?理由是: ;
(5)操作④的目的是: 。
(1)除去NH4HCO3,NH4HCO3 ==NH3↑+CO2↑+H2O;
(2)否,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,后面操作中无法除去;
(3)取上层清液加入BaCl2溶液,若无沉淀说明SO42-除尽;
(4)除去过量的Ba2+,减少一次过滤操作;
(5)除去溶解在溶液中的CO2及HCl;
【解析】
试题分析:(1)NH4HCO3加热易分解而除去,发生NH4HCO3 ==NH3↑+CO2↑+H2O;故答案为:除去NH4HCO3;(2)除杂时不能引入新的杂质,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,后面操作中无法除去,故答案为:否,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,后面操作中无法除去;(3)判断SO42-已除尽,可取上层清液加入BaCl2溶液,若无沉淀说明SO42-除尽,故答案为:取上层清液加入BaCl2溶液,若无沉淀说明SO42-除尽;(4)为避免重复操作,可先加入碳酸钠溶液,生成碳酸钡沉淀,减少实验的操作步骤,故答案为:除去过量的Ba2+,减少一次过滤操作;(5)反应后溶液中加入盐酸,生成二氧化碳气体,加热可除去溶解在溶液中的CO2及HCl,得到较为纯净的氯化钠溶液,故答案为:除去溶解在溶液中的CO2及HCl
考点:物质的分离提纯的实验方案的设计,物质分离和提纯的基本实验操作。


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:2014秋季湖南省高二上学期第一次阶段测试化学(B)试卷(解析版) 题型:选择题
对于密闭容器中进行的反应:2NO2  N2O4,下列说法正确的是
N2O4,下列说法正确的是
A.增大NO2的浓度,平衡常数增大
B.增大N2O4的浓度,平衡常数增大
C.增大NO2的浓度,正反应速率加快,逆反应速率减慢
D.增大NO2的浓度,平衡常数不变
查看答案和解析>>
科目:高中化学 来源:2015届广东省肇庆市高三一模理综化学试卷(解析版) 题型:选择题
下列各组离子能在水溶液中大量共存的是
A.H+、Fe2+、ClO-、SO42- B.Na+、Cu2+、S2-、ClO-
C.Na+、Ba2+、OH-、NO3- D.Na+、Al3+、SiO32-、CO32-
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:填空题
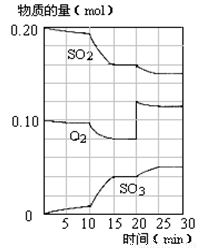
(16分)在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+ O2 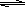 2SO3
2SO3
(1)已知:64g SO2完全转化为SO3会放出85kJ热量。 SO2转化为SO3的热化学方程式是 。
(2)该反应的化学平衡常数表达式K= 。
(3)降低温度,化学反应速率 。该反应K值将 。(填“增大”或“减小”或“不变”)
(4)450℃时,在一密闭容器中,将二氧化硫与氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
a.10-15min b.15-20min c.20-25min d.25-30min
(5)据图判断,10min到15min的曲线变化的原因可能是 (填写编号)。
a.增加SO3的物质的量 b.增大容器体积 c.降低温度 d.催化剂
(6)在15分钟时,SO2的转化率是 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高三第一次月考理综化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 NaOH溶液:K+、Ba2+、Cl-、HCO3-
B.0.1 mol·L-1 Na2CO3溶液:K+、NH 、NO
、NO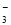 、SO
、SO
C.0.1 mol·L-1 FeCl3溶液:K+、Na+、I-、SCN-
D.0.1 mol·L-1 HCl的溶液:Ca2+、Na+、ClO-、NO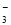
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高一第一学期期中考试化学试卷(解析版) 题型:选择题
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的Fe2(SO4)3、ZnSO4和K2SO4三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A.1∶2∶3 B.3∶2∶2 C.3∶1∶1 D. 1∶3∶3
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市高一第一学期期中考试化学试卷(解析版) 题型:选择题
张青莲是我国著名的化学家,1991年他准确测得In的相对原子质量为114.818,被国际相对原子质量委员会采用为新的标准值。这是相对原子质量表中首次采用我国测定的相对原子质量值。则下列关于的说法中,错误的是
A. In原子核外有49个电子
In原子核外有49个电子
B. In原子核内有49个中子
In原子核内有49个中子
C. In原子核内质子数和中子数之和等于其质量数为115
In原子核内质子数和中子数之和等于其质量数为115
D. In是In元素的一种核素
In是In元素的一种核素
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
鉴定NaCl的最佳方法是
A、焰色反应呈黄色,加硝酸酸化的AgNO3溶液有白色沉淀
B、焰色反应呈紫色,加盐酸酸化的AgNO3溶液有白色沉淀
C、焰色反应呈黄色,加盐酸酸化的AgNO3溶液有白色沉淀
D、焰色反应呈紫色,加硝酸酸化的AgNO3溶液有白色沉淀
查看答案和解析>>
科目:高中化学 来源:2015届江苏省、常州一中、沭阳中学高三联合调研化学试卷(解析版) 题型:选择题
(12分)金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。
(1)工业上处理酸性含Cr2O72-废水的方法如下:
①向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+。写出该反应的离子方程式: 。
②调节溶液的pH,使Cr3+完全沉淀。实验室粗略测定溶液pH的方法为
;25℃,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为 mol/L。(已知25℃时,Ksp[Cr(OH)3]=6.3×10-31)
(2)铬元素总浓度的测定:准确移取25.00mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后,以淀粉为指示剂,向其中滴加0.015mol/L的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mL。
计算废水中铬元素总浓度(单位:mg·L-1,写出计算过程)。
已知测定过程中发生的反应如下:
①2Cr3+ + 3S2O82- + 7H2O Cr2O72- + 6SO42- + 14H+
Cr2O72- + 6SO42- + 14H+
②Cr2O72- + 6I- + 14H+ 2Cr3+ + 3I2 + 7H2O
2Cr3+ + 3I2 + 7H2O
③I2 + 2S2O32- 2I- + S4O62-
2I- + S4O62-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com