
分析 (1)先计算出5min内Z的物质的量变化,根据物质的量与化学计量数成正比计算出n;
(2)根据化学反应速率与化学计量数成正比计算出前5min内用X表示的反应速率;
(3)根据Z的物质的量变化及Z与Y的计量数关系计算出5min内消耗Y的物质的量,然后计算出5min时Y的物质的量,最后根据c=$\frac{n}{V}$计算出5min末Y的浓度.
解答 解:(1)Z浓度变化来表示的平均速率为 0.03mol•L-1•min-1,则Z的物质的量变化为:0.03mol•L-1•min-1×2L×5min=0.3mol,根据物质的量之比等于计量数之比可知,n:2=0.3mol:0.2mol,解得;n=3,
故答案为:3;
(2)Z与X的化学计量数都是3,则前5min内用X表示的反应速率与Z表示的反应速率相等,都是0.03mol•(L•min)-1,
故答案为:0.03mol•(L•min)-1;
(3)5min内Z的物质的量变化为:0.03mol•L-1•min-1×2L×5min=0.3mol,根据反应3X(g)+Y(g)═3Z(g)+2W(g)可知5min末总共消耗Y的物质的量为:0.3mol×$\frac{1}{3}$=0.1mol,则5min末剩余Y的物质的量为:0.4mol-0.1mol=0.3mol,
所以5min末Y的物质的量浓度为:$\frac{0.3mol}{2L}$=0.15molL,
故答案为:0.15mol/L.
点评 本题考查了化学平衡、化学反应速率的计算,题目难度中等,明确化学反应速率的概念及表达式为解答关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
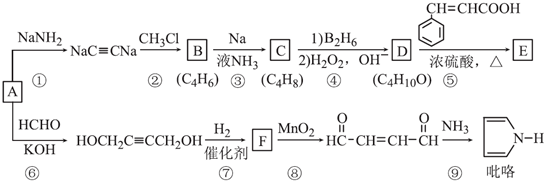
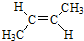 .
.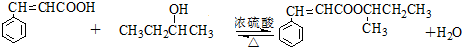 .
.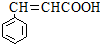 )的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有7种(不考虑顺反异构).与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是CH3CH2OCH2CH3.
)的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有7种(不考虑顺反异构).与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是CH3CH2OCH2CH3.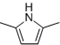 )的合成路线
)的合成路线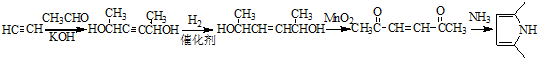 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③④ | C. | ④⑤ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D>A>B>C | B. | A>D>B>C | C. | D>A>C>B | D. | C>B>A>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将某气体燃烧,在火焰的上方罩一个冷而干燥的烧杯,烧杯内壁有水珠生成,再将烧杯立即倒转并加入澄清石灰水溶液震荡,石灰水变浑浊,则该气体一定是烃 | |
| B. | 除去乙酸乙酯中少量的乙酸,用饱和的碳酸钠溶液洗涤,然后分液、干燥、蒸馏 | |
| C. | 1ml 1%的NaOH溶液中加入2ml 2%的CuSO4溶液,振荡后再加入0.5ml淀粉的水解液,加热后未出现砖红色沉淀,说明淀粉尚未水解 | |
| D. | 乙酸和乙醇的酯化反应实验中,向试管中加入试剂的顺序是:浓硫酸、乙醇、冰醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴极上有Cu析出 | |
| B. | 阴极上产生的气体是氢气 | |
| C. | 阳极上产生的气体是氯气和氧气混合气体 | |
| D. | 使溶液恢复到原来状态,需加人适量CuO并通适量HC1气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
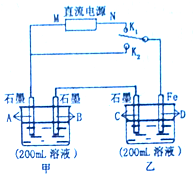 如图所示,甲、乙两个烧杯中的溶液中溶质离子分别由Na+、Cu2+、Cl-、SO42-四种离子中的一种阳离子和一种阴离子组成.(每种离子只能选用一次)
如图所示,甲、乙两个烧杯中的溶液中溶质离子分别由Na+、Cu2+、Cl-、SO42-四种离子中的一种阳离子和一种阴离子组成.(每种离子只能选用一次)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com