
| A. | ①③⑤⑦ | B. | ②④⑥⑦ | C. | ①③④⑤⑦ | D. | 全部都是 |
分析 原子和分子中核外电子数等于核内质子数,阴阳离子中核外电子数和核内质子数不同,两种微粒的质子数和电子数均分别相等,因中性微粒中质子数等于电子数,则两种微粒可能均为分子、原子,也可能为分子、原子,但离子中质子数一定不等于电子数,据此分析解答.
解答 解:①两种不同的原子互为同位素,它们的原子含有相同的质子数和电子数,如1H、2H,故①不选;
②原子中核外电子数等于核内质子数,两种元素的原子质子数和电子数都不同,故②选;
③可以是一种原子和一种分子,如Ne和HF的质子数、电子数均为10,则一种原子和一种分子的质子数和电子数均分别相等,故③不选;
④原子中核外电子数等于核内质子数,离子中核外电子数不等于核内质子数,所以一种原子和一种离子不可能质子数和电子数都相等,故④选;
⑤含有相同质子数和电子数的两种微粒,可以为电中性微粒,可能为不同的分子,如:NH3、H2O,故⑤不选;
⑥分子的质子数等于电子数,阳离子的电子数等于质子数减去电荷数,所以二者不可能质子数和电子数均分别相等,故⑥选;
⑦阳离子中核内质子数>核外电子数,阴离子中核内质子数<核外电子数,所以一种阳离子和一种阴离子只要质子数相同时,电子数就不同,故⑦选;
故选B.
点评 本题考查了核内质子数和核外电子数的关系,题目难度不大,明确阴阳离子中核外电子数与核内质子数的关系.


科目:高中化学 来源: 题型:选择题
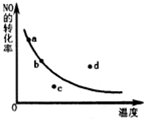 已知反应:2NO+O2?2NO2△H<0,如图曲线是表示其他条件一定时,反应中NO最大转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是( )
已知反应:2NO+O2?2NO2△H<0,如图曲线是表示其他条件一定时,反应中NO最大转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是( )| A. | a点 | B. | b点 | C. | c点 | D. | d点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1 mol N2(g)和 1 mol O2(g)反应放出的能量为 180 kJ | |
| B. | 1 mol N2(g)和 1 mol O2(g)具有的总能量小于 2 mol NO(g)具有的总能量 | |
| C. | 通常情况下,N2(g)和 O2(g)混合能直接生成 NO(g) | |
| D. | NO 是一种酸性氧化物,能与 NaOH 溶液反应生成盐和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为除去苯中的苯酚,可加入少量溴水溶液,再过滤 | |
| B. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| C. | 为除去乙炔气中少量的H2S,可使其通过CuSO4溶液 | |
| D. | 为除去CO2中少量的SO2,可使其通过饱和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中阴离子向正极移动 | |
| B. | 溶液中阴离子物质的量减少 | |
| C. | 负极的电极反应式是:N2H4+4OH--4e-═4H2O+N2↑ | |
| D. | 正极的电极反应式是:O2+4H++4e-═2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
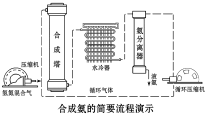 氨在国民经济中占有很重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.氨氧化法制硝酸是工业上制硝酸的主要方法.
氨在国民经济中占有很重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.氨氧化法制硝酸是工业上制硝酸的主要方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=4 | |
| B. | 每有3 mol Fe2+参加反应,反应中转移的电子总数为5 mol | |
| C. | 将Y均匀分散到水中形成的体系具有丁达尔效应 | |
| D. | S2O32-是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由氢气燃烧放热可知,2mol氢气的能量高于2mol水的能量 | |
| B. | 燃烧天然气做饭时,其能量转化形式只有化学能转化为热能 | |
| C. | 已知碳酸钙分解为吸热反应,则CaO与CO2反应为放热反应 | |
| D. | 根据能量守恒定律分析钠在氯气中燃烧的反应可知,参与反应的钠与氯气的总能量等于生成的氯化钠的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA | |
| B. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| C. | 标准状况下,2.24 L Cl2溶于水中达到饱和,转移的电子数是0.1NA | |
| D. | 25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com