
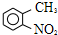
 路线如下:
路线如下: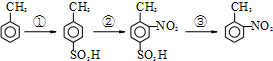 (反应条件略).推测该路线中磺酸基的作用防止甲基对位被硝基取代.
(反应条件略).推测该路线中磺酸基的作用防止甲基对位被硝基取代.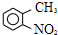 互为同分异构体,并同时满足下列条件的有机物有
互为同分异构体,并同时满足下列条件的有机物有 (写结构简式).
(写结构简式).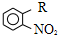 为原料,制取
为原料,制取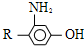 ,-R 基为d(填编号,下同)最合适;反应的合理顺序是f→e.
,-R 基为d(填编号,下同)最合适;反应的合理顺序是f→e. 合成
合成 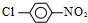 的化学方程式
的化学方程式 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,
+HCl, $→_{△}^{浓硝酸、浓硫酸}$
$→_{△}^{浓硝酸、浓硫酸}$ +H2O.
+H2O. 分析 (1)-CH3使新的取代基进入它的邻位或对位;
(2) 的同分异构体既能与酸反应,也能与碱反应,且该同分异构体与NaOH反应物质的量之比为1:2,说明含有氨基、羧酸与酚形成的酯基,且苯环上的一卤取代物有4种,取代基为-NH2、-OOCH处于邻位或间位;
的同分异构体既能与酸反应,也能与碱反应,且该同分异构体与NaOH反应物质的量之比为1:2,说明含有氨基、羧酸与酚形成的酯基,且苯环上的一卤取代物有4种,取代基为-NH2、-OOCH处于邻位或间位;
(3)由“取代基空间结构越大,邻位取代的可能越小”应选择空间结构大的取代基;
合成中苯环上的取代基应使新取代基加入相同的位置;
(4)-Cl使新取代基进入它的邻位或对位,而-NO2新取代基进入它的间位,应先由苯与氯气发生取代反应生成氯苯,然后氯苯与浓硝酸、浓硫酸在加热条件下发生取代反应.
解答 解:(1)-CH3使新的取代基进入它的邻位或对位,该路线中磺酸基的作用是:防止甲基对位被硝基取代,
故答案为:防止甲基对位被硝基取代;
(2) 的同分异构体既能与酸反应,也能与碱反应,且该同分异构体与NaOH反应物质的量之比为1:2,说明含有氨基、羧酸与酚形成的酯基,且苯环上的一卤取代物有4种,取代基为-NH2、-OOCH处于邻位或间位,可能的结构简式为:
的同分异构体既能与酸反应,也能与碱反应,且该同分异构体与NaOH反应物质的量之比为1:2,说明含有氨基、羧酸与酚形成的酯基,且苯环上的一卤取代物有4种,取代基为-NH2、-OOCH处于邻位或间位,可能的结构简式为: ,
,
故答案为: ;
;
(3)由“取代基空间结构越大,邻位取代的可能越小”应选择空间结构大的取代基,故选择-C(CH3)3,
由于-NH2、烃基使新取代基进入它的邻位或对位,而-NO2新取代基进入它的间位,使新取代基加入相同的位置,应先引入羟基,再将硝基还原为氨基,
故答案为:d;f、e;
(4)-Cl使新取代基进入它的邻位或对位,而-NO2新取代基进入它的间位,应先由苯与氯气发生取代反应生成氯苯,然后氯苯与浓硝酸、浓硫酸在加热条件下发生取代反应,反应方程式为: +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,
+HCl, $→_{△}^{浓硝酸、浓硫酸}$
$→_{△}^{浓硝酸、浓硫酸}$ +H2O,
+H2O,
故答案为: +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ +HCl,
+HCl, $→_{△}^{浓硝酸、浓硫酸}$
$→_{△}^{浓硝酸、浓硫酸}$ +H2O.
+H2O.
点评 本题考查信息的获取与迁移运用、限制条件同分异构体书写、有机物的合成等,旨在考查学生自学能力、分析推理能力,是有机化学常考题型.


科目:高中化学 来源: 题型:选择题
| A. | S(s) | B. | S(g) | C. | SO2(l) | D. | SO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子. ;Z2Y2与水反应放出气体的离子方程式为Na2O2+2H2O=4Na++4OH-+O2↑.
;Z2Y2与水反应放出气体的离子方程式为Na2O2+2H2O=4Na++4OH-+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用滤纸称量NaOH固体 | B. | 移液前容量瓶内有水珠 | ||
| C. | 摇匀后,液面低于刻度线 | D. | 定容时,俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
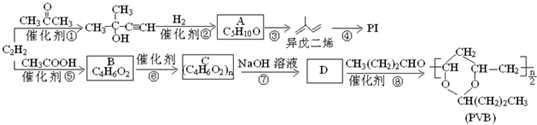

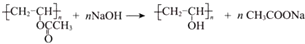 .
. ”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是
”改为“乙醛”,经过②、③、④后得到以顺式结构为主的高聚物,则用结构简式表示其顺式结构是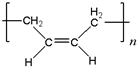 .
.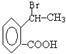 为原料合成
为原料合成 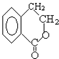 ,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式.
,下列是合成流程图,在括号内注明反应条件,方框内写出有关物质的结构简式.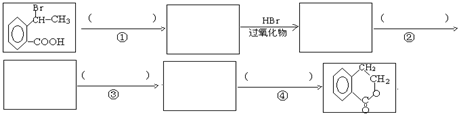
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
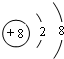 ;
;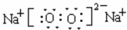 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液加入试管中, 加入过量的2mol/L盐酸,再滴加适量1mol/LBaCl2溶液 | 有白色沉淀生成, 证明待测液中含SO42-. |
| 步骤② | 另取少量待测液于试管中,加入足量氯水,再加入四氯化碳,震荡,静置后观察颜色 | 下层出现红棕色,则证明 待测液中含有:Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ③④②①⑥⑤ | C. | ①③④②⑥⑤ | D. | ③①④②⑥⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 投入铝粉产生H2的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 澄清透明的溶液中:Cu2+、SO42-、K+、NO3- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Cl- | |
| D. | 中性的溶液中:Al3+、Na+、SO42-、AlO2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com