
NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。

(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是_________________________。
(2)Ⅱ中,2NO(g)+O2(g)  2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。

①比较p1、p2的大小关系:________。
②随温度升高,该反应平衡常数变化的趋势是________。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g)  N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2
N2O4(l) ΔH2
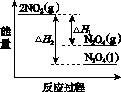
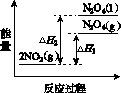
下列能量变化示意图中,正确的是(选填字母)________。

A B C
②N2O4与O2、H2O化合的化学方程式是________________________________________。
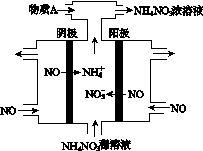
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充A。A是________,说明理由:________________________________________。
(1)4NH3+5O2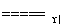 4NO+6H2O
4NO+6H2O
(2)①p1<p2 ②减小
(3)①A ②2N2O4+O2+2H2O===4HNO3
(4)NH3 根据反应:8NO+7H2O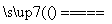 3NH4NO3+2HNO3,电解产生的HNO3多
3NH4NO3+2HNO3,电解产生的HNO3多
[解析] (1)氨的催化氧化的反应方程式为
4NH3+5O2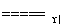 4NO+6H2O。
4NO+6H2O。
(2)①由2NO(g)+O2(g)  2NO2(g)可知该反应为气体体积减小的反应,温度相同,增大压强,平衡正向移动,NO的平衡转化率增大,根据图示和坐标含义,判断p1<p2;②再看同一压强线,温度升高,NO的平衡转化率降低,平衡向逆反应方向移动,则正反应为放热反应,温度升高,平衡常数减小。
2NO2(g)可知该反应为气体体积减小的反应,温度相同,增大压强,平衡正向移动,NO的平衡转化率增大,根据图示和坐标含义,判断p1<p2;②再看同一压强线,温度升高,NO的平衡转化率降低,平衡向逆反应方向移动,则正反应为放热反应,温度升高,平衡常数减小。
(3)①降低温度,NO2(g)转变为N2O4(l),则ΔH2<0,反应物能量高于生成物能量,C错误; N2O4(g)转变为N2O4(l)需要放出热量,所以NO2(g)转变为N2O4(g)比NO2(g)转变为N2O4(l)放出的热量少,B错误,所以正确的图示为A;②N2O4、O2和H2O反应生成硝酸的反应方程式为2N2O4+ O2+2H2O===4HNO3。
(4)根据工作原理装置图,可以确定阳极为NO失去电子转变为NO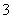 ,阴极NO转变为NH
,阴极NO转变为NH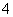 ,根据电极反应书写电极反应式为:
,根据电极反应书写电极反应式为:
阳极:NO-3e-+2H2O===NO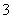 +4H+
+4H+
阴极:NO+5e-+ 6H+===NH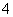 + H2O
+ H2O
然后根据得失电子守恒,硝酸根离子物质的量比铵根离子物质的量多,所以需要向溶液中加入的物质为NH3(即8NO+7H2O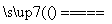 3NH4NO3+2HNO3)。
3NH4NO3+2HNO3)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法错误的是
A.0.1mol某醛与足量的银氨溶液反应,产生银的质量为21.6g,则该醛肯定为二元醛
B.乙醇、苯酚、乙酸都有羟基,但是电离常数不同,这主要是基团之间相互影响造成的
C. 分子中最多19个碳原子共平面、最多6个原子共直线
分子中最多19个碳原子共平面、最多6个原子共直线
D.分子式为C10H20O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C,则有机物A的可能结构有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除杂方案错误的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A. | CO(g) | CO2(g) | NaOH溶液、 浓H2SO4 | 洗气 |
| B. | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C. | Cl2(g) | HCl(g) | 饱和食盐水、 浓H2SO4 | 洗气 |
| D. | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.锥形瓶可用作加热的反应器
B.室温下,不能将浓硫酸盛放在铁桶中
C.配制溶液定容时,俯视容量瓶刻度会使溶液浓度偏高
D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制备下列气体时,所用方法正确的是( )
A.制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置
B.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体
C.制乙烯时,用排水法或向上排空气法收集气体
D.制二氧化氮时,用水或NaOH溶液吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质应用的说法错误的是( )
A.玻璃容器可长期盛放各种酸
B.纯碱可用于清洗油污
C.浓氨水可检验氯气管道漏气
D.Na2S可除去污水中的Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关硅的叙述中,正确的是( )
A.工业上通常以SiO2为原料,用氧化剂与其反应制备单质硅
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各选项能说明分子式为C4H6的某烃是HC≡C—CH2—CH3,而不是CH2===CH—CH===CH2的事实是( )
A.燃烧时有浓烟
B.能使酸性KMnO4溶液褪色
C.所有原子不在同一平面上
D.与足量溴水反应,生成物中只有2个碳原子上有溴原子
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:
(1)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 kJ。该反应的热化学方程式为____________________________________________。
(2)反应AX3(g)+X2(g)  AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
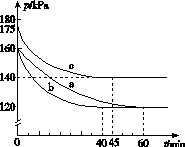
①列式计算实验a从反应开始至达到平衡时的反应速率v(AX5)=______________________。
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为____________(填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b________________________________________________,c____________________________________________。
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为______________;实验a和c的平衡转化率:αa为________,αc为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com