
【题目】科学家在 20℃时,将水置于足够强的电场中,水分子瞬间凝固成“暖冰”。对“暖冰”与其它物质比较正确的是( )
A.与Na2O 晶体类型相同B.与![]() 化学键类型相同
化学键类型相同
C.与CO2 分子构型相同D.与 CH4 分子极性相同
【答案】B
【解析】
根据题干信息,将水置于足够强的电场中,水分子瞬间凝固成“暖冰”,该过程时物理变化,分子没有发生改变,“暖冰”还是水分子,据此分析解答。
A.“暖冰”中H2O分子为分子晶体,Na2O是离子晶体,两者晶体类型不同,A选项错误;
B.“暖冰”中H2O分子中H原子和O原子之间形成极性共价键,SiO2中Si原子和O原子形成极性共价键,两者化学键类型相同,B选项正确;
C.“暖冰”中H2O分子中O原子的价电子对数为![]() ,有两对孤电子对,其分子构型为V形,CO2中C原子的价电子对数为
,有两对孤电子对,其分子构型为V形,CO2中C原子的价电子对数为![]() ,没有孤电子对,分子构型为直线形,两者分子构型不同,C选项错误;
,没有孤电子对,分子构型为直线形,两者分子构型不同,C选项错误;
D.“暖冰”中H2O分子中O原子的价电子对数为![]() ,有两对孤电子对,而CH4分子中C原子的价电子对数为
,有两对孤电子对,而CH4分子中C原子的价电子对数为![]() ,不存在孤电子对,两者分子极性不同,D选项错误;
,不存在孤电子对,两者分子极性不同,D选项错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】现有mA(s)+nB(g)qC(g) △H<0的可逆反应,在一定温度下达平衡时,B的体积分数ф(B)和压强p的关系如图所示,则下列有关该反应的描述正确的是( )

A. m+n<qB. n>q
C. x点的混合物中v (正)<v (逆)D. x点比y点的混合物的正反应速率小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E分别是铁或铁的化合物。其中D是一种红褐色沉淀。其相互反应关系如图所示:

根据如图所示变化,按要求回答下列问题:
(1)写出A、E的化学式:A__,E__;
(2)写出其中几步反应的化学方程式:
C→B:___;
B→D:___;
E→A:___。
(3)C中加入NaOH溶液,看到的现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知六种物质:①H2O ②氨水③ Mg ④ HNO3 ⑤Ba(OH)2 ⑥CuSO4·5H2O
根据上述提供的物质,回答下列问题:
(1)属于电解质的是________(填序号,下同)。
(2)上述物质中④与⑤反应的离子方程式为_________。
(3)实验室配制900mL 0.1mol/L硫酸铜溶液,需要称取的溶质(从上述物质中选取)的质量为________g。在配制过程中,若其它操作均正确,则下列操作会使所配溶液物质的量浓度偏低的是_________(填字母序号)。
A 溶解后小烧杯、玻璃棒没有洗涤
B 所用容量瓶中,已有少量蒸馏水
C 定容摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
D 定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
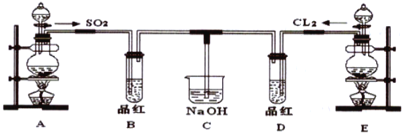
(1)写出Cu与浓硫酸制备SO2的化学方程式__________。
(2)实验室用装置E制备Cl2的离子方程式_________ 。指出该反应中HCl(浓)所表现出的化学性质__________、___________。
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现__________的现象。
A品红都褪色 B品红都不褪色
C试管B 中品红褪色D 中不褪色 D试管D 中品红褪色B 中不褪色
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象又分别为_____。
A 无色 红色 B 无色 无色 C 红色 红色 D 红色 无色
(4)C烧杯氢氧化钠溶液的作用是___________。
(5)另一个实验小组的同学认为SO2 和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下的密闭容器中:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=-905.9kJ·mol-1。下列叙述正确的是
4NO(g)+6H2O(g) △H=-905.9kJ·mol-1。下列叙述正确的是
A.4molNH3和5molO2反应,达到平衡时放出热量为905.9kJ
B.平衡时,5v正(O2)=4v逆(NO)
C.平衡后降低压强,混合气体平均摩尔质量增大
D.平衡后升高温度,混合气体中NO含量降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式______,____。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气体,则该漂白粉中所含有效成份的质量为_____________(假设漂白粉中的其它成份不与硝酸反应)。
(2)将14 g Na2O和Na2O2的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶液的体积为400 mL。试计算:原混合物中Na2O的质量为______g,所得溶液的物质的量浓度为______ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇脱水是合成环己烯的常用方法,实验室合成环己烯的反应和实验装置如图:
![]()

可能用到的有关数据如下:

Ⅰ.合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5 %碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是__。
(2)加入碎瓷片的作用是__;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是__(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并__;在本实验分离过程中,产物应该从分液漏斗的__(填“上口倒出”或“下口倒出”)。
(4)分离提纯过程中加入无水氯化钙的目的是__。
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有__(填正确答案标号)。
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() 某一元碱
某一元碱![]() 与
与![]() 盐酸反应,反应过程中由水电离的
盐酸反应,反应过程中由水电离的![]() 浓度的负对数
浓度的负对数![]() 与所加盐酸的体积间关系如图,下列说法正确的是( )
与所加盐酸的体积间关系如图,下列说法正确的是( )
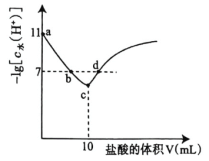
A.水的电离程度![]()
B.![]() 点溶液满足
点溶液满足![]()
C.![]() 为弱碱,其电离平衡常数
为弱碱,其电离平衡常数![]() 约为
约为![]()
D.![]() 点溶液满足
点溶液满足![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com