
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是
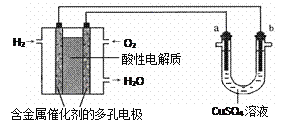
A. 燃料电池工作时,通入氢气的是正极
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g), 已知反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol; 反应达平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%。则:
2NH3(g), 已知反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol; 反应达平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%。则:
(1)a的值为______。
(2)平衡时NH3的物质的量为___________。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=___________________。
(4)原混合气体中,a∶b=________。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=________。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于反应:2SO2(g)+O2(g)![]() 2SO3 (g) ,下面表示该反应速率最快的是_______。
2SO3 (g) ,下面表示该反应速率最快的是_______。
A.v(SO2)= 2 mol/(L·min) B.v(O2)=1mol/(L·min)
C.v(O2)=2mol/(L·min) D.v(SO3)= 3mol/(L·min)
(2)下图表示在密闭容器中反应:2SO2(g)+O2(g)![]() 2SO3 (g) ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a b过程中改变的条件是______________;
2SO3 (g) ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a b过程中改变的条件是______________;
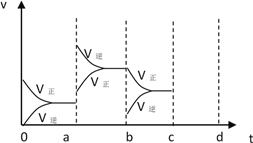
b c过程表示平衡向_______方向移动; 若增大压强时,反应速率变化情况画在下图c~d处______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去苯中混有的少量甲苯,下列的实验正确的是( )
A.在分液漏斗中,加入足量溴水,充分震荡后,静置分液分离
B.使用蒸馏烧瓶,加热蒸馏出苯
C.在烧杯中,加入足量烧碱溶液,充分搅拌后,转移至分液漏斗,静置分液分离
D.在分液漏斗中,加入足量酸性高锰酸钾溶液,充分搅拌后,静置分液分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关碱金属和卤素的说法正确的是( )
A. 从Li到Cs,单质的熔、沸点越来越高
B. 从F到I,单质与H2化合生成的氢化物越来越稳定
C. 从F到I,前一种单质都能把后一种单质从其盐溶液中置换出来
D. 从Li到Cs,最高价氧化物对应的水化物碱性越来越强,单质与水反应越来越剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g)。反应的平衡常数如下表:
CH3OH(g)。反应的平衡常数如下表:
温度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
下列说法正确的是
A. 该反应的△H>0
B. 加压、增大H2浓度和加入催化剂都能提高CO的转化率
C. 工业上采用高温高压的条件,目的都是提高原料气的转化率
D. t℃时,向1 L密闭容器中投入0.1 mol CO和0.2 mol H2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 mol·L-1的CH3COOH溶液中,下列关系正确的是
A. c(CH3COOH)>c(H+)>c(CH3COO-) >c(OH-)
B. c(CH3COO-)>c(CH3COOH>c(H+) >c(OH-)
C. c(CH3COOH)>c(CH3COO-)=c (H+)>c(OH-)
D. c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若ABn的中心原子A上没有孤对电子,运用价层电子对互斥模型,下列说法正确的是
A. 若n=2,则分子的立体结构为V形
B. 若n=3,则分子的立体结构为三角锥形
C. 若n=4,则分子的立体结构为正四面体形
D. 以上说法都不正确
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com