
���� ��1����KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
��n��Fe��=$\frac{11.2g}{56g/mol}$=0.2mol���ɷ�Ӧ��֪����COΪ0.2mol��$\frac{3}{2}$=0.3mol�����v=$\frac{��c}{��t}$���㣻
��2������Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ���������䣬ע��÷�Ӧ��һ����Ӧǰ�������������Ļ�ѧ��Ӧ�����Բ�����ѹǿ�ж�ƽ�⣻
��3��������֪�Ȼ�ѧ����ʽ�����ø�˹���ɼ������д�Ȼ�ѧ����ʽ��
��� �⣺��1������Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g���������岻�ܴ���K�ı���ʽ�У���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=$\frac{{c}^{3}��C{O}_{2}��}{{c}^{3}��CO��}$��
�ʴ�Ϊ��$\frac{{c}^{3}��C{O}_{2}��}{{c}^{3}��CO��}$��
��n��Fe��=$\frac{11.2g}{56g/mol}$=0.2mol���ɷ�Ӧ��֪����COΪ0.2mol��$\frac{3}{2}$=0.3mol����10min��CO��ƽ����Ӧ����Ϊv=$\frac{��c}{��t}$=$\frac{\frac{0.3mol}{2L}}{10min}$=0.015mol/��L��min����
�ʴ�Ϊ��0.015mol/��L��min����
��2��Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
a��CO��CO2�������������������������˵����Ӧ�ﵽƽ��״̬����a��ȷ��
b��CO����CO2�����������ٸı䣬���ʵ������䣮˵��Ũ�Ȳ��䣬��b��ȷ��
c��һ����̼�Ͷ�����̼��Ӧ�Ķ�����ϵΪ1��1��CO����CO2�����������50%����˵����Ӧ�ﵽƽ��״̬����c����
�ʴ�Ϊ��a b��
��3������֪�Ȼ�ѧ����ʽ��
2 I2��s��+5O2��g��=2 I2O5��s������H=-75.56kJ•mol-1�٣�
2CO��g��+O2��g��=2 CO2��g������H=-566.0kJ•mol-1�ڣ�
���ݸ�˹���ɽ�����ʽ�ڡ�$\frac{5}{2}$-�١�$\frac{1}{2}$��5CO��g��+I2O5��s��=5 CO2��g��+I2��s����H=��-566.0kJ•mol-1����$\frac{5}{2}$-��-75.56kJ•mol-1����$\frac{1}{2}$=-1377.22kJ/mol��
�������Ȼ�ѧ��Ӧ����ʽΪ��5CO��g��+I2O5��s��=5 CO2��g��+I2��s����H=-1377.22kJ/mol��
�ʴ�Ϊ��5CO��g��+I2O5��s��=5 CO2��g��+I2��s����H=-1377.22kJ/mol��
�ʴ�Ϊ��5CO��g��+I2O5��s��=5CO2��g��+I2��s����H=-1377.22kJ•mol-1��
���� ���⿼�����Ȼ�ѧ����ʽ����д��������ѧƽ��ļ�������жϣ�ƽ���־�ķ������жϣ�����ƽ���ƶ�ԭ���ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
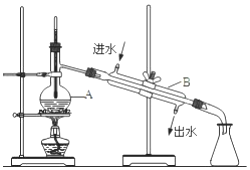 ��ͼΪʵ�����Ʊ�����ˮ��װ��ʾ��ͼ������ͼʾ�ش��������⣮
��ͼΪʵ�����Ʊ�����ˮ��װ��ʾ��ͼ������ͼʾ�ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͨ�����з�ɢϵ���г����Ŀ�����������īˮ���ܹ۲쵽�����ЧӦ | |
| B�� | ��Һ�����塢��Һ�ĸ��������Ƿ�ɢ����ֱ���Ĵ�С | |
| C�� | ��1mL0.1mol/L���Ȼ�����Һ�μ���20mL��ˮ�У��ӱ������Ƶ������������� | |
| D�� | ������ȶ��Խ�����Һ����Һ֮�䣬���ڽ�����ϵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
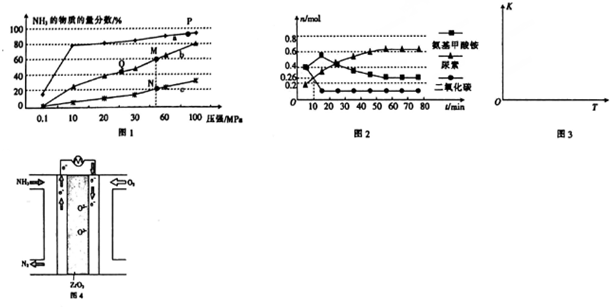
 һ�������£����ݻ�Ϊ3L���ܱ������У�������ӦCO��g��+2H2��g��?CH3OH��g����H��0���ڲ�ͬ�¶��¼״������ʵ�����ʱ��ı仯��ͼ��ʾ������������ȷ���ǣ�������
һ�������£����ݻ�Ϊ3L���ܱ������У�������ӦCO��g��+2H2��g��?CH3OH��g����H��0���ڲ�ͬ�¶��¼״������ʵ�����ʱ��ı仯��ͼ��ʾ������������ȷ���ǣ�������| A�� | ƽ�ⳣ��K��300�棩��K��500�棩 | |
| B�� | 500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��=$\frac{nB}{3tB}$ mol•L-1•min-1 | |
| C�� | �������������������£�������E�����ϵ���ݻ�ѹ����ԭ����$\frac{1}{2}$��������Ũ�ȼ�С | |
| D�� | 300�棬��������ѹǿ����ʱ˵����Ӧ�Ѿ��ﵽƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��ú��������Һ����ýྻ��ȼ�� | |
| B�� | �ӿ���ܡ�̫���ܡ�����������Դ�Ŀ������� | |
| C�� | ������Դ���ģ�ע����Դ���ظ�ʹ�á���Դ��ѭ������ | |
| D�� | ������չũ���������������Ľո�ת��Ϊ����Ч����Դ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
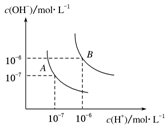 ˮ�ĵ���ƽ��������ͼ��ʾ����A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ���100��ʱ1mol•L-1��NaOH��Һ�У���ˮ�������c��H+��=1��10-12mol•L-1��KW��25�棩��KW��100�棩�����������������=������
ˮ�ĵ���ƽ��������ͼ��ʾ����A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ���100��ʱ1mol•L-1��NaOH��Һ�У���ˮ�������c��H+��=1��10-12mol•L-1��KW��25�棩��KW��100�棩�����������������=�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | OH-�����ʵ��� | B�� | c��H+�� c��OH-�� | C�� | c��NH4+�� | D�� | c��OH-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com