
下列离子方程式书写正确的是( )
|
| A. | 氯气跟水反应:Cl2+H2O=2H++Cl﹣+ClO﹣ |
|
| B. | 硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42﹣=BaSO4↓ |
|
| C. | 碳酸钠溶液中加入少量稀盐酸:CO32﹣+H+=HCO3﹣ |
|
| D. | 铜与稀盐酸反应:Cu+2H+=Cu2++H2↑ |
| 离子方程式的书写. | |
| 分析: | A.次氯酸为弱电解质,保留化学式; B.漏掉了铜离子与氢氧根离子的反应; C.碳酸钠溶液中加入少量稀盐酸反应生成碳酸氢钠; D.铜与盐酸不反应. |
| 解答: | 解:A.氯气跟水反应,离子方程式:Cl2+H2O=H++Cl﹣+HClO,故A错误; B.硫酸铜溶液跟氢氧化钡溶液反应,离子方程式:2H++2OH﹣+Ba2++SO42﹣=BaSO4↓+2H2O,故B错误; C.碳酸钠溶液中加入少量稀盐酸,离子方程式:CO32﹣+H+=HCO3﹣,故C正确; D.铜与盐酸不反应,故D错误; 故选:C. |
| 点评: | 本题考查了离子方程式的书写,明确反应的实质是解题关键,注意碳酸根于氢离子反应的过程,为易错点. |


科目:高中化学 来源: 题型:
25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为
0.1000 mol·L-1的三种酸HX、HY、HZ滴定曲线如图所示。
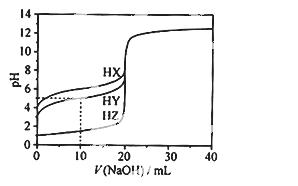
下列说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:
c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)=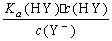 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一容积可变的容器中,反应2A(g)+B(g)⇌2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol.保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡左移的是( )
|
| A. | 均减半 | B. | 均加倍 | C. | 均增加1mol | D. | 均减少1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应:M(g)+N(g)⇌P(g)+Q(g)△H>0,请回答下列问题.
(1)在某温度下,反应物的起始浓度分别为:c(M)=1mol•L﹣1,c(N)=2.4mol•L﹣1,达到平衡后,M的转化率为60%,此时N的转化率为 .
(2)若反应温度升高,M的转化率 (填“增大”、“减小”或“不变”)
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4mol•L﹣1,c(N)=amol•L﹣1;达到平衡后,c(P)=2mol•L﹣1,a= .
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)=b mol•L﹣1,达到平衡后,M的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
|
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的杀菌净化 |
|
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
|
| C. | MgO的熔点很高,可用于制作耐高温材料 |
|
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和④ B.①和③ C.③和④ D.①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学用某种粗盐进行提纯实验,步骤见下图。
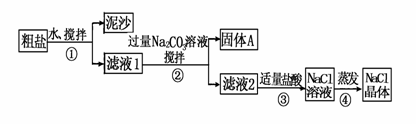
请回答:
(1)步骤①和②的操作名称是________________。
(2)步骤③判断加入盐酸“适量”的方法是___________________________
步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止_________________,当蒸发皿中有较多量固体出现时,应__________________,用余热使水分蒸干。
(3)猜想和验证,请完成下表:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 |
| 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入 ,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 |
|
| 猜想Ⅲ:最后制得的NaCl固体中还含有Na2SO4 | 取少量NaCl固体溶于试管中的蒸馏水, 。 |
| 猜想Ⅲ成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现代循环经济要求综合考虑环境污染和经济效益。请填写下列空白:
(1)实验室里,可用于吸收SO2尾气的一种试剂是 。
(2)高纯氧化铁可作现代电子工业材料。以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁(软磁α-Fe2O3)的生产流程示意图:


①步骤Ⅰ中过滤所得滤渣的主要成分是 。
②步骤Ⅱ 中加入铁粉的目的是 。
中加入铁粉的目的是 。
③步骤Ⅲ中可选用________试剂调节溶液的pH(填标号)。
A.稀硝酸 B.双氧水 C.氨水 D.高锰酸钾溶液
④写出在空气中煅烧FeCO3,制备高纯氧化铁的化学方程式:____________________。
⑤从滤液C中回收的主要物质的一种用途是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com