
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,下列有关说法正确的是( )
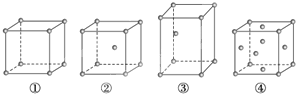
A. ①为简单立方堆积,②为镁型,③为钾型,④为铜型
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
(1)将钠、铝、钾各 1mol 分别投入到足量的相同浓度的盐酸中,试预测实验结果:与盐酸 反应最剧烈的单质是 , 与盐酸反应产生的气体最多的是 .
(2)向 Na2S 溶液中通入氯气出现黄色浑浊,可证明 Cl 的非金属性比 S 强,反应离子方程式 为 .
(3)利用如图装置可验证同主族元素非金属性的变化规律:仪器 A 的名称为 , 装置 D 的作用为; 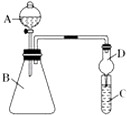
①若要证明非金属性:Cl>I,则 A 中加浓盐酸,B 中加 KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C 中加淀粉碘化钾混合溶液,观察到 C 中溶液的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气.
②若要证明非金属性:C>Si,则在 A 中加盐酸、B 中加 CaCO3、C 中加 Na2SiO3 溶液,观察到 C 中溶液的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入 C 中干扰实验,应在两装置间添加装有溶液的洗气瓶.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(原创)下列物质分类正确的是
A.SO2、SiO2、P2O5均为酸性氧化物
B.是否具有丁达尔效应是胶体与溶液、浊液的根本区别
C.纯净盐酸为纯净物、冰水混合物为混合物
D.烧碱、纯碱都属于碱,油脂、甘油都属于酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电子排布式或轨道表示式正确的是
A. C原子的轨道表示式:![]()
B. Ca原子的电子排布式:1s22s22p63s23p63d2
C. N原子的轨道表示式:![]()
D. Br-的电子排布式[Ar] 3d104s24p6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C为短周期元素,在周期表中所处的位置如表所示.
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)写出B,C元素的名称、 .
(2)B位于元素周期表中第周期第族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是 , 质量为g,电解的总反应方程式为;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
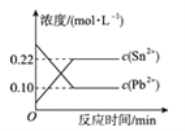
A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
C. 25 ℃时,该反应的平衡常数K=2.2
D. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 0.1mol/L氨水中,c(OH-)=c(NH4+)
B. 在常温下,10mL 0.02mol/L HCl溶液与10mL 0.02mol.LBa(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12
C. 新制氯水中c(Cl-)=c(ClO-)+c(HClO)
D. 0.1mol/L KHC2O4溶液显酸性,溶液中c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(H2C2O4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com