
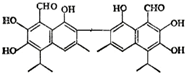
 �������̨�������������������۵�ijƷ�Ƽ���Ϊ����Ƥ���������������ʤ��ƹ���������Ϊ�漦����ר�ҽ��ܣ��������ڼ����������������ѱ����Ӷ�ʹ�����ﺬ�й��������£���ṹ��ʽ��ͼ��ʾ������˵������ȷ���ǣ�������
�������̨�������������������۵�ijƷ�Ƽ���Ϊ����Ƥ���������������ʤ��ƹ���������Ϊ�漦����ר�ҽ��ܣ��������ڼ����������������ѱ����Ӷ�ʹ�����ﺬ�й��������£���ṹ��ʽ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | �û�����ķ���ʽΪ��C30H30O8 | |
| B�� | 1mol��������10mol H2�ӳɣ���6molNaOH��Ӧ | |
| C�� | ��һ�������£��������ᷴӦ������������ | |
| D�� | �����ʿ���ʹ���Ը��������Һ��ɫ |
���� �ɽṹ��֪����ʽ�������к���-OH��-CHO����������Ϸӡ�ȩ���������������
��� �⣺A���ɽṹ��֪���û�����ķ���ʽΪ��C30H30O8����A��ȷ��
B��������-CHO�������������ӳɷ�Ӧ��1mol��������12mol H2�ӳɣ�ֻ�з�-OH��NaOH��Ӧ����6molNaOH��Ӧ����B����
C����-OH������ɷ���������Ӧ�����������ʣ���C��ȷ��
D����-OH��-CHO���뱽��������C����H�����ɱ����Ը��������Һ����ʹ����ɫ����D��ȷ��
��ѡB��
���� ���⿼���л���Ľṹ�����ʣ�Ϊ��Ƶ���㣬�����л���Ĺ����������ʵĹ�ϵΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע������ŵ��жϣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʣ�࣬����Һ���ٵ���������������ܽ⣬Ҳ���ܲ��ܽ� | |
| B�� | ������ȫ���ܽ⣬����Һ��һ������Fe3+ | |
| C�� | ������ȫ���ܽ⣬�Ҳ���336 mL���壨��״��������b=0.3 | |
| D�� | ����Һ�н�������ֻ��Fe3+��Cu2+ʱ����a��b�Ĺ�ϵΪ��b��80y��1-$\frac{a}{3}$�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��3���ڽ���Ԫ������������Ӧ��ˮ����������ԭ����������������� | |
| B�� | ����At���ǵڢ�A��Ԫ�أ����⻯����ȶ��Դ���HCl | |
| C�� | ��2���ڷǽ���Ԫ�ص���̬�⻯������ˮ��ˮ��Һ��Ϊ���� | |
| D�� | �裨Tl������ͬ���壬�䵥�ʼ��������ᷴӦ������������������Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| T | ��������ˮ���ҷ�Ӧ��������Һ�������� |
| X | ԭ�������������Ǵ�����3�� |
| Y | ��������Ԫ�صļ������а뾶��С |
| Z | ��̬�⻯��������������Ӧˮ����ɷ������Ϸ�Ӧ |
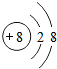 ��д��Ԫ��Z�ĵ��ʵĵ���ʽ
��д��Ԫ��Z�ĵ��ʵĵ���ʽ ����Ԫ�ط��ű�ʾ��
����Ԫ�ط��ű�ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������



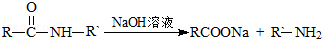
 ��ת��Ϊ1mol A��1molB����A��FeCl3��Һ��������ɫ��д��A��ϡ��Һ�����Ũ��ˮ������Ӧ�Ļ�ѧ����ʽ��
��ת��Ϊ1mol A��1molB����A��FeCl3��Һ��������ɫ��д��A��ϡ��Һ�����Ũ��ˮ������Ӧ�Ļ�ѧ����ʽ�� ��
��  ������Ϣʹ�Ľṹ��ʽΪ
������Ϣʹ�Ľṹ��ʽΪ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ��������ˮ | |
| B�� | ͨ�����������Ը��������Һ | |
| C�� | ȼ�� | |
| D�� | ʹ��Ȳ��һ�������������������ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������д��ģ�̻����裬����̻���� | |
| B�� | �����յ�����ˮ��������ˮ�ռ�ϵͳ���������ˮ��Դ | |
| C�� | ���������������ռ��������м��з��մ��� | |
| D�� | �ڽ�������չ����Ӫ������Ӧ�ô��ģ��̫���ܹ������ϵͳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com