
| A. | (CH3)3CCH2OH | B. | 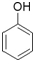 | C. | 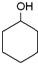 | D. | (CH3)2CBrCH2OH |
分析 连接醇羟基的碳原子上含有两个H原子的醇能发生催化氧化反应生成醛,连接醇羟基或卤原子的碳原子相邻碳原子上含有H原子的有机物能发生消去反应,据此分析解答.
解答 解:连接醇羟基的碳原子上含有两个H原子的醇能发生催化氧化反应生成醛,连接醇羟基或卤原子的碳原子相邻碳原子上含有H原子的有机物能发生消去反应,
A.该分子能被催化氧化生成醛,但不能发生消去反应,故A错误;
B.该分子不能发生催化氧化反应也不能发生消去反应,故B错误;
C.该分子发生催化氧化反应生成酮而不能生成醛,故C错误;
D.该分子中连接醇羟基的碳原子上含有2个氢原子,所以能发生催化氧化生成醛,连接溴原子的碳原子相邻碳原子上含有H原子,所以能发生消去反应,故D正确;
故选D.
点评 本题考查消去反应和醇的催化氧化反应,为高频考点,明确有机物官能团和性质关系是解本题关键,注意醇发生催化氧化反应及消去反应结构特点,题目难度不大.


科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol丙烯中含有共价键的数目为0.6NA | |
| B. | 0.1mo Cl2全部溶于水后转移电子的数目为0.1NA | |
| C. | 标准状况下,2.24LSO3中含有氧原子的数目为0.3NA | |
| D. | 9.2g由乙醇和二甲醚(CH3OCH3)组成的混合物中含有氧原子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
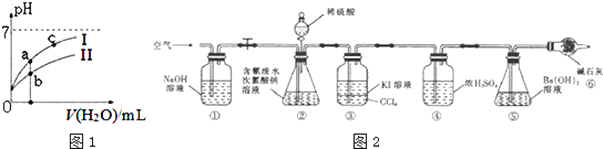
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数( 25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
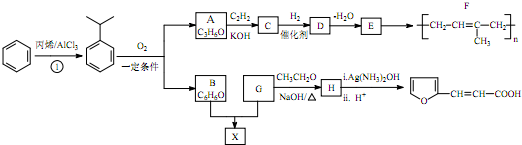
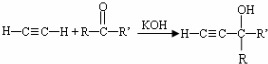
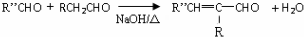 (-R、-R′、-R″表示可能相同或可能不同的原子或原子团)
(-R、-R′、-R″表示可能相同或可能不同的原子或原子团)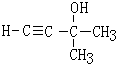 .
.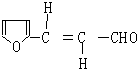 ,H的同分异构体中属于芳香族化合物的共有5种.
,H的同分异构体中属于芳香族化合物的共有5种.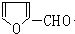 +CH3CHO$→_{△}^{NaOH}$
+CH3CHO$→_{△}^{NaOH}$ +H2O.
+H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯醛的结构简式:CH2═CHCHO | |
| B. | CSO的电子式: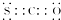 | |
| C. | 硫酸氢钠熔融时的电离方程式:NaHSO4═Na++HSO4- | |
| D. | S2-的结构示意图: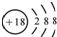 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 25℃时,pH=4.5的硫酸溶液中c(H+) 是pH=5.5的磷酸中c(H+)的10倍 | |
| B. | 因为合金在潮湿的空气中易形成原电池,所以合金的耐腐蚀性都较差 | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 | |
| D. | 常温下,2NO(g)+O2(g)?2NO2(g)能够自发进行,则该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1 mol/LCH3COONa溶液与0.1 mol/LCaCl2溶液等体积混合:c(Na+)+c(Ca2+)═c(CH3COO-)+c(CH3COOH)+2c(Cl- ) | |
| B. | 将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体后的溶液:c(H+)+c(H2CO3)═c(OH-)+c(CO32-)+c(NH3•H2O) | |
| C. | 0.1 mol/LCH3COONa溶液与0.1 mol/LHCl溶液混合至pH=7:c(Na+)>c(Cl-)=c(CH3COOH)>c(CH3COO-) | |
| D. | 0.2mol/L氨水与0.1 mol/LHCl溶液等体积混合:c(Cl-)+c(H+)═c(NH3•H2O)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅的非金属性比硫弱 | B. | 硅酸钠可溶于水 | ||
| C. | SiO2与氢氟酸能反应 | D. | 硅原子易失去或得到电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com