
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
方法a | 用炭粉在高温条件下还原CuO |
方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O |
方法c | 电解法,反应为2Cu + H2O |
方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)已知:①2Cu(s)+![]() O2(g)=Cu2O(s)△H = -169kJ·mol-1,②C(s)+
O2(g)=Cu2O(s)△H = -169kJ·mol-1,②C(s)+![]() O2(g)=CO(g)△H = -110.5kJ·mol-1,③ Cu(s)+
O2(g)=CO(g)△H = -110.5kJ·mol-1,③ Cu(s)+![]() O2(g)=CuO(s)△H = -157kJ·mol-1,则方法a发生的热化学方程式是:____________。
O2(g)=CuO(s)△H = -157kJ·mol-1,则方法a发生的热化学方程式是:____________。
(2)方法c采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示:
该离子交换膜为____离子交换膜(填“阴”或“阳”),该电池的阳极反应式为_____,钛极附近的pH值________(填“增大”“减小”或“不变”)。

(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为________。
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:![]() △H>0。水蒸气的浓度随时间t变化如下表所示:
△H>0。水蒸气的浓度随时间t变化如下表所示:
序号 | 0 | 10 | 20 | 30 | 40 | 50 | |
① | p>T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
①对比实验的温度:T2_________T1(填“﹥”“﹤”或“﹦”),能否通过对比实验①③到达平衡所需时间长短判断:_________(填 “能”或“否”)。
②实验①前20 min的平均反应速率 v(O2)=_________
③催化剂的催化效率:实验①___________实验②(填“﹥”或“﹤”)。
【答案】2CuO(s)+C(s)=Cu2O(s)+CO(g) ΔH=+34.5kJ/mol 阴 2Cu-2e-+2OH-= Cu2O+H2O 增大 4Cu(OH)2+N2H4![]() 2Cu2O+6H2O+N2↑ > 否 3.5×10-5 mol/(L·min) <
2Cu2O+6H2O+N2↑ > 否 3.5×10-5 mol/(L·min) <
【解析】
(1)用碳还原CuO,发生的化学方程式是2CuO(s)+C(s)=Cu2O(s)+CO(g),根据盖斯定律,可知该反应的反应热为①+②-2×③=(-169kJ·mol-1)+(-110.5kJ·mol-1)-2×(-157kJ·mol-1)=+34.5kJ/mol,则方法a发生的热化学方程式是2CuO(s)+C(s)=Cu2O(s)+CO(g) ΔH=+34. 5kJ/mol,故答案为:2CuO(s)+C(s)=Cu2O(s)+CO(g) ΔH=+34.5kJ/mol;
(2)该电解池的阳极发生氧化反应,所以Cu失去电子,与氢氧根离子结合生成氧化亚铜和水,电极反应式是2Cu-2e-+2OH-=Cu2O+H2O;钛极为阴极,氢离子放电生成氢气,则氢氧根离子浓度增大,所以钛极附近的pH值增大,故答案为:阴;2Cu-2e-+2OH-=Cu2O+H2O;增大;
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2,根据元素守恒可知,还有水生成,则化学方程式是4Cu(OH)2 + N2H4 ![]() 2Cu2O + 6H2O + N2↑,故答案为:4Cu(OH)2 + N2H4
2Cu2O + 6H2O + N2↑,故答案为:4Cu(OH)2 + N2H4 ![]() 2Cu2O + 6H2O + N2↑;
2Cu2O + 6H2O + N2↑;
(4)①T2时20min即达平衡状态,所以T2的反应速率快,则T2>T1,由于①③实验中的起始浓度不同,所以不能通过对比实验①③到达平衡所需时间长短判断,故答案为:>;否;
②实验①前20 min内水蒸气的浓度减小(0.05-0.0486)mol/L=0.0014mol/L,则氧气的浓度增加0.0007mol/L,所以前20min内的平均反应速率v(O2)=0.0007mol/L÷20min=3.5×10-5mol·L-1min-1,故答案为:3.5×10-5mol·L-1min-1;
③①与②相比,达到的平衡状态相同,但②达到平衡的时间短,所以②的反应速率快,则实验②比实验①所用的催化剂催化效率高,故答案为:<。
【点晴】
影响化学反应速率的因素有多种,在探究相关规律时,需要控制其他条件不变,只改变某一个条件,探究这一条件对反应速率的影响。变量探究实验因为能够考查学生对于图表的观察、分析以及处理实验数据归纳得出合理结论的能力,因而在这几年高考试题中有所考查。解答此类题时,要认真审题,清楚实验目的,弄清要探究的外界条件有哪些。然后分析题给图表,确定一个变化的量,弄清在其他几个量不变的情况下,这个变化量对实验结果的影响,进而总结出规律,然后再确定另一个变量,重新进行相关分析。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:
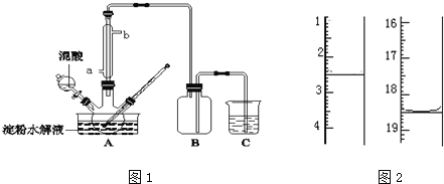
①将1:1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体,硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的作用是:_________;
(2)实验中若混酸滴加过快,将导致草酸产量下降,其原因是_________;
(3)检验淀粉是否水解完全所用的试剂为_________;
(4)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有_________;
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸.用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O称取该样品0.12g,加适量水完全溶解,然后用0.020molL﹣1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时溶液颜色变化为_________,滴定前后滴定管中的液面读数如图2所示,则该草酸晶体样品中二水合草酸的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,正确的是
A.甲烷的燃烧热△H=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ/mol
B.一定条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热akJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) △H=-2akJ/mol
2NH3(g) △H=-2akJ/mol
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ/mol
D.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=-114.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
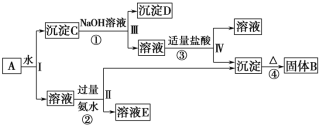
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是__。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
固体B__;沉淀C__;沉淀D__;溶液E___。
(3)写出①、②、③、④四个反应的化学方程式或离子方程式
①__;
②___;
③___;
④__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共用两个及两个以上碳原子的多环烃称为桥环烃,共用的碳原子称为桥头碳。桥环烃二环[2.2.0]己烷的碳原子编号为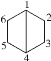 。下列关于该化合物的说法错误的是( )
。下列关于该化合物的说法错误的是( )
A.桥头碳为1号和4号
B.与环己烯互为同分异构体
C.二氯代物有6种(不考虑立体异构)
D.所有碳原子不可能位于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】杯环芳烃因其结构类似于酒杯而得名,其键线式如图,下列关于杯环芳烃的说法正确的是( )
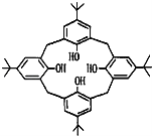
A.属于芳香烃B.最多与6mol H2发生加成反应
C.分子式为C44H56O4D.分子内所有原子一定在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是一种活泼的金属,在高温下能与Fe2O3反应生成Fe和Al2O3。该反应中___________(填化学式)是还原剂,_____________(填化学式)氧化剂。当2molFe2O3参加反应时,转移了 ____________ mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:

试回答下列问题:
①图1的A中最好选用下列装置_________(填编号);
②图1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
④某学生按图2进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________,其反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2011年9月23日,中国科学家屠呦呦获得了美国拉斯克医学奖的临床医学奖,获奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”。下图是青蒿素的结构,则有关青蒿素的说法中不正确的是:

A.青蒿素分子式为C15H22O5
B.青蒿素有—O—O—键具有较强的氧化性
C.青蒿素易溶于水、乙醇、苯
D.青蒿素在碱性条件下易发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com