
| A. | ①④ | B. | ②⑤ | C. | ②③④⑤ | D. | ①②③④ |
分析 ①分馏时温度计用于测量馏分的温度;
②溴水与二氧化硫发生氧化还原反应;
③应该使用浓硫酸,否则该反应不会发生;
④苯和溴水不发生反应;
⑤为减缓反应的速率,可用饱和食盐水与电石反应.
解答 解:①分馏时温度计用于测量馏分的温度,温度计的水银球应放在蒸馏烧瓶的支管口,故①错误;
②溴水与二氧化硫发生氧化还原反应,而乙烷不与溴水反应,可以用溴水除去乙烷中的二氧化硫,故②正确;
③乙醇的消去反应必须使用浓硫酸,稀硫酸不能起到催化作用,故③错误;
④苯和溴水不反应,应该用液溴,故④错误;
⑤为减缓反应的速率,可用饱和食盐水与电石反应,故⑤正确;
故选B.
点评 本题考查较为综合,涉及物质的分离、提纯、制备等知识,综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:解答题

| 温度/溶解度/盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46g NO2和N2O4的混合气体中含有的原子个数为3NA | |
| B. | 常温下,4 g CH4含有NA个C-H共价键 | |
| C. | 10 mL质量分数为98%的H2SO4,加水至100 mL,H2SO4的质量分数为9.8% | |
| D. | 25℃时,pH=12的1.0 LNaClO溶液中水电离出的OH-的数目为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 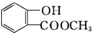 | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关 | |
| B. | H2O的熔、沸点高于H2S是由于H2O分子之间存在氢键 | |
| C. | I2易溶于CCl4可以用相似相溶原理解释 | |
| D. | 甲烷可与水形成氢键这种化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
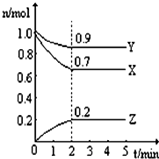 某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示,由图中数据分析:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:实验题

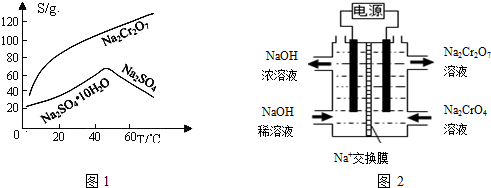
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com