
设NA 为阿伏加德罗常数的值。下列说法正确的是( )
A.1 L 0.1 mol•L-1的氨水含有0.1NA个OH-
B.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
C.25 ℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0 .1 NA
D.在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数为NA
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
下列说法正确的是
A.化学反应中的能量变化,只表现为热量的变化
B.煤和石油属于可再生能源
C.汽车排出大量尾气中含有CO会污染大气
D.要使燃料燃烧只需要大量的氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
A.用物质A表示的反应平均速率为0.3 mol·L-1·s-1
B.用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
C.2 s时物质A的转化率为70%
D.2 s时物质B的浓度为0.7 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两只试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是____________________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH______1(选填“>”、“<”或“=”);乙方案中,说明HA是弱电解质的现象是_______。
a.装HCl 溶液的试管中放出H2的速率快
溶液的试管中放出H2的速率快
b.装HA溶液的试管中放出H2的速率快
c.两只试管中产生气体速率一样快
(3)请你评价:乙方案中难以实现之处或不妥之处_________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是( )
A.c(OH-) B.c(H+) C.中和时所需NaOH的量 D.c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度时于密封容器中发生反应:mA(g)+nB(g)  pC(g),达平衡后,若将气体体积扩大到原来的2倍。再达平衡时A的浓度是原来的0.8倍,则下列叙述正确的是( )
pC(g),达平衡后,若将气体体积扩大到原来的2倍。再达平衡时A的浓度是原来的0.8倍,则下列叙述正确的是( )
A.平衡向正向移动 B.新平衡时,v正(A)=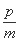 v逆(C)
v逆(C)
C.气体A的转化率升高 D.m+n>p
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应原理及其应用,不正确的是( )
A.苯与浓硝酸反应;制备TNT炸药
B.葡萄糖能与新制Cu(OH)2悬浊液反应;尿糖检测
C.醋酸能与CaCO3、Mg(OH)2等反应;用食醋除去暖瓶中的水垢
D.乙烯能与水反应生成乙醇;制取工业酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)(2013·宜春模拟)①含0.4 mol Al3+的Al2(SO4)3中所含的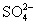 的物质的量是______________。
的物质的量是______________。
②2.3 g Na中含电子的物质的量为 mol,在跟足量水反应中失去电子的物质的量为 mol。
(2)(2013·阜新模拟)①48 g 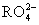 中,核外电子总数比质子总数多6.02×1023个,则R元素的摩尔质量为 。
中,核外电子总数比质子总数多6.02×1023个,则R元素的摩尔质量为 。
②有一真空瓶的质量为M1 g,该瓶充入空气后总质量为M2 g;在相同状况下,若改充某气体A后,总质量为M3 g,则A的相对分子质量为 。
(3)(2013· 江西师大附中模拟)一定量的氢气在氯气中燃烧,所得混合物用
100 mL 3.00 mol·L-1的NaOH溶液(密度为1.12 g·mL-1)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.050 0 mol。
①原NaOH溶液的质量分数为___________________________;
②所得溶液中Cl-的物质的量为_________________________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com