
物质的量浓度相同的①氨水、②氯化铵、③碳酸氢铵、④硫酸氢铵、⑤硫酸铵5种溶液中[NH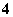 ]的大小顺序是____________________,溶液pH的大小顺序是________________________________________________________________________。
]的大小顺序是____________________,溶液pH的大小顺序是________________________________________________________________________。
⑤>④>②>③>①
①>③>②>⑤>④
解析 本题可分3种情况讨论:(1)氨水电离产生NH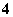 、OH-;(2)NH
、OH-;(2)NH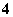 水解产生H+及剩余NH
水解产生H+及剩余NH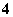 ;(3)NH
;(3)NH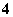 水解受到影响,促进或抑制。在分析时要注意两点:氨水电离程度不是很大,NH
水解受到影响,促进或抑制。在分析时要注意两点:氨水电离程度不是很大,NH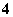 水解程度也不是很大。另外,NH4HSO4溶液,H+抑制NH
水解程度也不是很大。另外,NH4HSO4溶液,H+抑制NH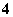 水解,而NH4HCO3中,HCO
水解,而NH4HCO3中,HCO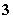 比氨水更弱,HCO
比氨水更弱,HCO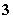 水解呈碱性,会促进NH
水解呈碱性,会促进NH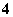 水解,但影响不是很大,(NH4)2SO4溶液中,NH
水解,但影响不是很大,(NH4)2SO4溶液中,NH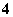 的浓度最大。所以,NH
的浓度最大。所以,NH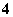 的浓度由大到小顺序为(NH4)2SO4、NH4HSO4、NH4Cl、NH4HCO3、NH3·H2O,其中pH可根据NH
的浓度由大到小顺序为(NH4)2SO4、NH4HSO4、NH4Cl、NH4HCO3、NH3·H2O,其中pH可根据NH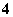 水解程度及电离的情况得出pH由大到小的顺序是NH3·H2O、NH4HCO3、NH4Cl、(NH4)2SO4、NH4HSO4。
水解程度及电离的情况得出pH由大到小的顺序是NH3·H2O、NH4HCO3、NH4Cl、(NH4)2SO4、NH4HSO4。


科目:高中化学 来源: 题型:
在50 mL 0.2 mol·L-1 CuSO4溶液中插入两个电极,通电电解(不考虑水分蒸发)。则:
(1)若两极均为铜片,试说明电解过程中CuSO4溶液的浓度________(填“增大”、“减小”或“不变”)。
(2)若阳极为纯锌,阴极为铜片,阳极反应式是________________________________________________________________________
________________________________________________________________________。
(3)若阳极为纯锌,阴极为铜片,如不考虑H+在阴极上放电,当电路中有0.04 mol e-通过时,阴极增重________g,阴极上的电极反应式是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量浓度、等体积的氢氧化钠溶液和醋酸溶液完全反应后,溶液中有关离子浓度之间不存在的关系是( )
A.[H+][OH-]=KW
B.[Na+]>[CH3COO-]>[OH-]>[H+]
C.[Na+]=[CH3COO-]+[OH-]
D.[Na+]+[H+]=[CH3COO-]+[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 Na2CO3溶液:[OH-]=[H+]+[HCO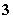 ]+2[H2CO3]
]+2[H2CO3]
B.0.1 mol·L-1 NH4Cl溶液:[NH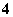 ]=[Cl-]
]=[Cl-]
C.向醋酸钠溶液中加入适量醋酸,得到酸性的混合溶液:
[Na+]>[CH3COO-]>[H+]>[OH-]
D.向硝酸钠溶液中滴加稀盐酸得到pH=5的混合溶液:
[Na+]=[NO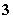 ]+[Cl-]
]+[Cl-]
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如右图,下列说法不正确的是( )。
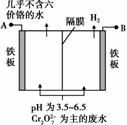
A.A接电源正极
B.阳极区溶液中发生的氧化还原反应为Cr2O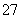 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
C.阴极区附近溶液pH降低
D.若不考虑气体的溶解,当收集到H2 13.44 L(标准状况)时,有0.1 mol Cr2O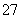 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
室温时,下列溶液中微粒的浓度关系正确的是 )。
A.0.1 mol·L-1 pH=4的NaHSO3溶液中:cHSO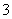 )>cSO
)>cSO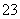 )>cH2SO3)
)>cH2SO3)
B.等体积、等物质的量浓度的NaF溶液与HF溶液混合:cNa+)=cF-)+cHF)
C.在NaHA溶液中一定有:cNa+)+cH+)=cHA-)+cOH-)+cA2-)
D.cNH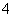 )相等的NH4)2CO3、NH4)2SO4和NH4)2FeSO4)2三份溶液中,溶质的物质的量浓度依次增大
)相等的NH4)2CO3、NH4)2SO4和NH4)2FeSO4)2三份溶液中,溶质的物质的量浓度依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应①:CO(g)+CuO(s)CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)Cu(s)+H2O(g)在相同温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=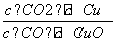
B.反应③的平衡常数K=K1/K2
C.对于反应③,恒容时,若温度升高,H2的浓度减小,则该反应的焓变为正值
D.对于反应③,恒温恒容时,若增大压强,H2的浓度一定减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com