
| A.是指常温常压下,2个氢分子和1个氧分子反应生成2个水分子,放出热量571.6 kJ |
| B.是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),放出热量571.6 kJ |
| C.是指标准状况下,2 mol H2O(l)分解为2 mol H2(g)和1 mol O2(g),吸收热量571.6 kJ |
| D.是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),放出热量571.6 kJ |
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
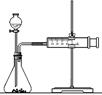
科目:高中化学 来源:不详 题型:实验题
| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③④⑤⑥ | B.②③④ |
| C.②⑤⑥ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.做该实验时环境温度为22℃ | B.该实验表明化学能可能转化为热能 |
| C.NaOH溶液的浓度约为1.0mol/L | D.该实验表明有水生成的反应都是放热反应 |
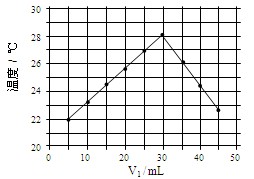
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
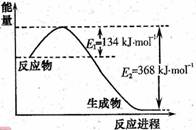
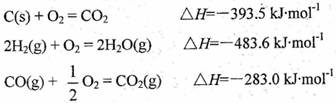
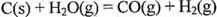 的焓变为 。
的焓变为 。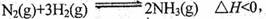 其化学平衡常数K与t的关系如下表:
其化学平衡常数K与t的关系如下表:
| A.容器内N2、H2、NH3的浓度之比为1:3:2 |
| B.2v(正)(N2)=v(逆)(H2) |
| C.容器内压强保持不变 |
| D.混合气体的密度保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应的ΔH2=+483.6kJ/mol | B.|ΔH2|<|ΔH1| |
| C.|ΔH2|>|ΔH1| | D.热化学方程式中化学计量数表示分子个数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
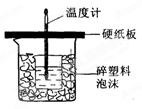
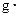 ℃),盐酸和NaOH溶液的密度认为都是1
℃),盐酸和NaOH溶液的密度认为都是1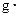
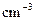 )
)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com