
| A. | 某溶液为蓝色,则该溶液一定是CuSO4溶液 | |
| B. | 向某溶液中加入Ba(NO3)2溶液无明显现象,再滴入几滴硝酸酸化的AgNO3溶液,产生白色沉淀,说明原溶液中含有Cl- | |
| C. | 向某溶液中加入CaCl2溶液,产生白色沉淀,则溶液中一定含有Ag+ | |
| D. | 加入稀HNO3酸化的BaCl2溶液,有白色沉淀生成,证明原溶液中一定有SO42- |
分析 A.含铜离子的溶液可为蓝色;
B.加入Ba(NO3)2溶液无明显现象,排除硫酸根离子、碳酸根离子等干扰,后滴入几滴硝酸酸化的AgNO3溶液,产生白色沉淀,白色沉淀为AgCl;
C.加入CaCl2溶液,产生白色沉淀,白色沉淀为AgCl或碳酸钙等;
D.白色沉淀为AgCl或硫酸钡.
解答 解:A.含铜离子的溶液可为蓝色,则某溶液为蓝色,则该溶液可能是CuSO4溶液或CuCl2溶液等,故A错误;
B.加入Ba(NO3)2溶液无明显现象,排除硫酸根离子、碳酸根离子等干扰,后滴入几滴硝酸酸化的AgNO3溶液,产生白色沉淀,白色沉淀为AgCl,则原溶液中含有Cl-,故B正确;
C.加入CaCl2溶液,产生白色沉淀,白色沉淀为AgCl或碳酸钙等,则溶液中可能含有Ag+或碳酸根离子等,但不能同时存在,故C错误;
D.白色沉淀为AgCl或硫酸钡,则原溶液中可能有SO42-或银离子,但二者不能同时存在,故D错误;
故选B.
点评 本题考查常见离子的检验,为高频考点,把握离子检验的试剂、现象、结论为解答的关键,侧重分析与实验能力的考查,注意检验时排除干扰离子,题目难度不大.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
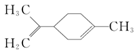 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )| A. | 它在核磁共振氢谱中有6个峰 | B. | 它能发生取代、加成和氧化反应 | ||
| C. | 它与丁基苯互为同分异构体 | D. | 它属于芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物油(水)与乙醇(水) | B. | 蛋白质溶液(NaCl)与淀粉溶液(KI) | ||
| C. | 泥水(淀粉溶液)与Fe(OH)3胶体(FeCl3) | D. | 氧化钙(碳酸钙)与NaHCO3 (Na2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取4g NaOH加入100mL水中配制浓度为1.0mol/L的NaOH溶液 | |
| B. | 配制一定浓度的溶液时,用蒸馏水润洗容量瓶会使所配制出的溶液浓度偏低 | |
| C. | 除去Fe(OH)3胶体中混有的Cl-离子,可用过滤的方法 | |
| D. | 向盛有铜片的试管中加入浓硫酸,加热证明浓硫酸具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取7.68gCuSO4,加入500mL水 | |
| B. | 称取12.5g胆矾,配成480mL溶液 | |
| C. | 称取8.0gCuSO4,加入到500mL水中配成溶液 | |
| D. | 称取12.5g胆矾,配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaAlO2溶液和盐酸 | B. | NaHCO3溶液和Ca(OH)2溶液 | ||
| C. | NaOH溶液和浓AlCl3溶液 | D. | 稀硫酸和碳酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuH与盐酸的反应属于置换反应 | |
| B. | CuH在Cl2中燃烧,1molCuH转移电子数为2NA | |
| C. | CuH在Cl2中燃烧时铜元素和氢元素均被氧化 | |
| D. | CuH与盐酸反应的离子方程式:H-+H+═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{49a}{b}$ mol-1 | B. | $\frac{49b}{a}$ mol-1 | C. | $\frac{98a}{b}$ mol-1 | D. | $\frac{98b}{a}$ mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
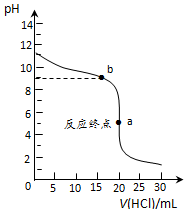
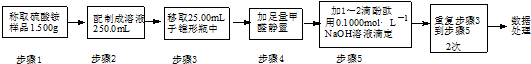
| 滴定次数 | 待测溶液的 体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 20.01 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.30 | 20.30 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com