
| A、常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3NA |
| B、标准状况下,22.4L SO3的分子数为NA |
| C、1molFe在22.4L的Cl2(标准状况下)燃烧,转移的电子总数为3NA |
| D、电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |


科目:高中化学 来源: 题型:

| A、A的分子式为:C14H13O5N2 |
| B、A可以发生水解反应、中和反应、加成反应、消去反应 |
| C、A物质完全水解的产物中,一定含有醇类 |
| D、在一定条件下,1molA最多能与1L 2mol?L-1NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁在海水中比在河水中更易腐蚀,主要原因是海水含盐量高于河水 |
| B、NaFeO4自身处理水的原理与明矾和漂白粉共同处理水的原理相同 |
| C、高温或日常用的消毒剂可使H7N9型禽流感病毒蛋白质变性 |
| D、“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br-、Fe2+、I- |
| B、Br-、I-、Fe2+ |
| C、I-、Fe2+、Br- |
| D、Fe2+、I-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA |
| B、1 L 0.1 mol.L-1的醋酸溶液中氢离子数为0.1 NA |
| C、以惰性电极电解NaCl溶液时,每放出11.2LCl2时,则消耗NaCl个数为NA |
| D、在密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移的电子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
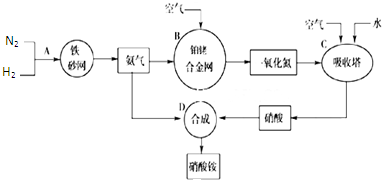
| ||
| △ |
| 注意事项 | 理由 | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水吸收足量的SO2气体:OH-+SO2=HSO3- |
| B、稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| C、用NaOH溶液吸收废气中氮氧化物:NO+NO2+OH-=NO2-+H2O |
| D、向碳酸氢钙溶液中加入少量的氢氧化钠溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
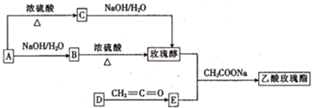
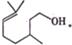

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com