
已知下列热化学方程式:
①CaCO3(s)===CaO+CO2(g) ΔH=177.7 kJ
②C(s)+H2O(s)===CO(g)+H2(g)
ΔH=-131.3 kJ·mol-1
③ H2SO4(l)+NaOH(l)===
H2SO4(l)+NaOH(l)=== Na2SO4(l)+H2O(l)
Na2SO4(l)+H2O(l)
ΔH=-57.3 kJ·mol-1
④C(s)+O2(g)===CO2(g)
ΔH=-393.5 kJ·mol-1
⑤CO(g)+ O2(g)===CO2(g)
O2(g)===CO2(g)
ΔH=-283 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)===2H2O(l)
ΔH=-517.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有_________________________________________,
不正确的理由分别是____________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式:
________________________________________________________________________。
(3)上述反应中,表示标准燃烧热的热化学方程式有________________________________;
表示中和热的热化学方程式有______________。
答案 (1)①②③
①中CaO没标状态,ΔH=177.7 kJ·mol-1;
②中H2O的状态应为“g”;
③中除H2O外其他物质的状态不是“l”应为“aq”
(2)C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
(3)④⑤ ⑥
解析 (2)④-⑤得:C(s)+ O2(g)===CO(g)
O2(g)===CO(g)
ΔH=-393.5 kJ·mol-1-(-283 kJ·mol-1)=-110.5 kJ·mol-1。
(3)标准燃烧热是指在101 kPa下,1 mol物质完全燃烧的反应热,故④⑤正确;⑦表示的不是1 mol H2的燃烧。中和热是指在稀溶液中,强酸跟强碱发生中和反应,生成 1 mol H2O(l)时的反应热,故⑥正确;③不正确,除H2O外其他物质的状态不是“l”而是“aq”。


科目:高中化学 来源: 题型:
化学式为C8Hm的烷烃,m值等于________;CnH22的烷烃,n值等于________;相对分子质量为212的烷烃的分子式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2A
 B+D在四种不同条件下进行。B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行。B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20 min时间内的平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=______mol·L-1,反应经20 min就达到了平衡,可推测实验2中还隐含的条件是____________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______v1(填“>”、“=”或“<”),且c3______1.0 mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应的正反应是______反应(填“吸热”或“放热”),理由是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 g H2完全燃烧生成水蒸气放出热量121 kJ,且O2中1 mol O===O键完全断裂时吸收热量496 kJ,水蒸气中形成1 mol H—O键时放出热量463 kJ,则H2中1 mol H—H键断裂时吸收的热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为O2+4e-+2H2O===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
要使工业废水中的重金属Pb2+离子沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,已知Pb2+离子与这些离子形成的化合物的溶解度如下:
| 化合物 | PbSO4 | PbCO3 | PbS |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 | 1.84×10-14 |
由上述数据可知,选用的沉淀剂最好为( )
A.硫化物 B.硫酸盐 C.碳酸盐 D.以上沉淀剂均可
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去MgCl2的酸性溶液中的Fe3+,可在加热条件下加入一种试剂,过滤后再加入一定量的盐酸,这种试剂是( )
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
星形聚合物SPLA可经下列反应路线得到(部分反应条件未注明)。
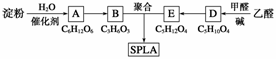
已知:SPLA的结构简式为
 ,其中R为
,其中R为
(1)淀粉是________糖(填“单”或“多”);A的名称是____________。
(2)乙醛由不饱和烃制备的方法之一是
________________________________________________________________________
________________________________________________________________________(用化学方程式表示,可多步)。
(3)D→E的化学反应类型属于________反应;D结构中有3个相同的基团,且1 mol D能与2 mol Ag(NH3)2OH反应,则D的结构简式是____________;D与银氨溶液反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(4)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO3溶液反应,又不能与新制Cu(OH)2悬浊液反应,且1 mol G与足量Na反应生成1 mol H2,则G的结构简式为________________________________________________________________________。
(5)B有多种脱水产物,其中两种产物的结构简式为____________________和
____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
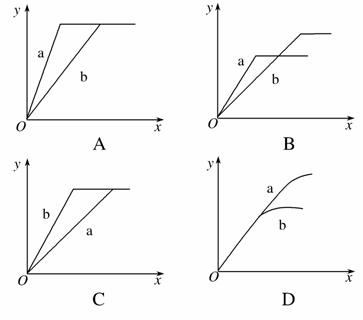
进行如下实验:在a锥形瓶中放入10 g绿豆粒大的碳酸钙,在b锥形瓶中放入5 g粉末状的碳酸钙,分别加入50 mL 1 mol·L-1的盐酸。图中(图中:x表示时间;y表示锥形瓶中碳酸钙减少的质量)能正确表示实验结果的是( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com