
【题目】铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+![]() CO(g)═
CO(g)═![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g)△H2
CO2(g)△H2
Fe3O4(s)+CO(g)═3Fe(s)+CO2(g)H3
Fe2O3(s)+CO(g)═2Fe(s)+3CO2(g)H4
则△H4的表达式为__________(用含△H1、△H2、△H3的代数式表示).
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为__________,该温度下若测得固体混合物中m(Fe):m(O)=35:2,则FeO被CO还原为Fe的百分率为__________(设其它固体杂质中不含Fe、O元素).
(3)铁等金属可用作CO与氢气反应的催化剂.已知某种催化剂可用来催化反应CO(g)+3H2(g)CH4(g)+H2O(g)△H<0.在T℃,106Pa时将lmolCO和3molH2加入体积可变的密闭容器中.实验测得CO的体积分数x(CO)如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断CO(g)+3H2(g)![]() CH4(g)+H2O(g)达到平衡的是__________(填序号).
CH4(g)+H2O(g)达到平衡的是__________(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为__________;在T℃106Pa时该反应的压强平衡常数Kp(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为__________;
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是__________,理由是__________。

【答案】(1)△H2+![]() △H3 ;(2)FeO和Fe;80%;(3)①bd;②37.1%;
△H3 ;(2)FeO和Fe;80%;(3)①bd;②37.1%;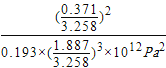 ;③T3>T2>T1;正反应放热,在相同压强下,温度降低,平衡向正反应方向移动,CO的转化率升高
;③T3>T2>T1;正反应放热,在相同压强下,温度降低,平衡向正反应方向移动,CO的转化率升高
【解析】
试题分析:(1)已知反应:Fe2O3(s)+![]() CO(g)═
CO(g)═![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g)△H2 ②Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H3 ③,根据盖斯定律,将所给的反应②+③×
CO2(g)△H2 ②Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H3 ③,根据盖斯定律,将所给的反应②+③×![]() 可得:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g),故△H4=△H2+
可得:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g),故△H4=△H2+![]() △H3 ,故答案为:△H2+
△H3 ,故答案为:△H2+![]() △H3 ;
△H3 ;
(2)根据当1000℃时为FeO,在2000℃时为Fe,故在1600℃时固体物质的主要成分为FeO和Fe的混合物;设混合物中FeO的物质的量为xmol,Fe的物质的量为ymol,则有:![]() =
=![]() ,即可求的x:y=1:4,故剩余的FeO和被还原为铁的FeO的物质的量之比为1:4,则可知被还原的FeO的百分比为
,即可求的x:y=1:4,故剩余的FeO和被还原为铁的FeO的物质的量之比为1:4,则可知被还原的FeO的百分比为![]() ×100%=80%,故答案为:FeO和Fe;80%;
×100%=80%,故答案为:FeO和Fe;80%;
(3)①a.由于此容器是个体积可变的容器,故为恒容的容器,则容器内压强一直不变,故不能作为反应达平衡的标志,故a错误;b.此反应在平衡前,气体的质量不变,但体积变小,故密度变大,故当混合气体的密度不再发生变化时能说明反应达平衡,故b正确;c.反应达平衡的根本标志是v正=v逆,所以3v正(CO)=v逆(H2),故c错误;d.在反应达平衡之前,混合气体的质量不变,但物质的量变小,故混合气体的平均相对分子质量在变小,故当不变时能说明反应达平衡,故d正确。故选bd;
②设反应达平衡时CO转化了xmol,则根据三段式可知:
CO(g) + 3H2(g)![]() CH4(g)+H2O(g)
CH4(g)+H2O(g)
初始(n): 1mol 3mol 0 0
△n: xmol 3xmol xmol xmol
平衡(n): (1-x)mol (3-3x)mol xmol
结合平衡时CO的体积分数为0.193可知:![]() =0.193,解得x=0.371,故达到平衡时CO的转化率为=
=0.193,解得x=0.371,故达到平衡时CO的转化率为=![]() ×100%=37.1%;在T℃106Pa时该反应的压强平衡常数Kp=
×100%=37.1%;在T℃106Pa时该反应的压强平衡常数Kp=![]() =
=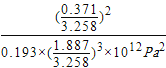 ,故答案为:37.1%;
,故答案为:37.1%;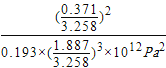 ;
;
③反应CO(g)+3H2(g)![]() CH4(g)+H2O(g)△H<0,温度越高,则平衡左移,CO的平衡转化率越低,根据图象可知,温度T3>T2>T1,故答案为:T3>T2>T1;正反应放热,在相同压强下,温度降低,平衡向正反应方向移动,CO的转化率越高。
CH4(g)+H2O(g)△H<0,温度越高,则平衡左移,CO的平衡转化率越低,根据图象可知,温度T3>T2>T1,故答案为:T3>T2>T1;正反应放热,在相同压强下,温度降低,平衡向正反应方向移动,CO的转化率越高。


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+ =2 Ag +Cu2+ ”设制一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是_______,发生_________反应(填“氧化”或“还原”),电解质溶液是_______;
(2)若导线上转移电子1 mol,则生成银___________克。
如图为某化学兴趣小组进行不同条件下化学能转变为电能探究的装置。请你回答下列问题:

(3)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:___________。
(4)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该装置___________(填“能”或“不能”)形成原电池,若不能,请说明理由;若能,请指出正、负极_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1体积CH4和4体积Cl2组成的混合气体充入大试管中。
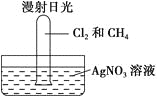
将此试管倒立在盛有AgNO3溶液的水槽中,放在光亮处,片刻后发现试管壁上有油状液滴出现,该油状液滴可能是________,水槽中还观察到________,原因是________(用离子方程式解释)。若向水槽中再滴入几滴紫色石蕊试液又观察到________,原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )


A. 图Ⅰ所示装置用于 Cu 和浓 H2SO4 制取少量的 SO2 气体
B. 图Ⅱ装置可验证非金属性:Cl>C>Si
C. 图Ⅲ可用于收集气体 H2、CO2、Cl2、NH3
D. 图Ⅳ表示将 SO2 气体通入 H2S 水溶液中,所得溶液的 pH 变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知部分弱酸的电离常数如下表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离常数(25 ℃) | Ka=1.8×10-5 | Ka=5.0×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
请回答下列问题:
(1)25 ℃时,在某二元酸 H2A 溶液中存在的所有微粒为:H+、OH-、HA-、A2-、H2O,写出 H2A 的 电离方程式_____。
(2)25 ℃时,在 0.5 mol·L-1 的醋酸溶液中由醋酸电离出的[H+]约是_________,是该溶液 中由水电离出的[H+]的_____倍,醋酸的电离度为_____(填百分数)
(3)写出向氰化钠溶液中通入少量二氧化碳的离子方程式:______________________________。
(4)25 ℃时,CH3COOH 与 CH3COONa 的混合溶液,若测得混合液 pH=6,则溶液中[CH3COO-]-[Na+]=_____(填准确数值)。
(5)25 ℃时,将 a mol·L-1 的醋酸与 b mol·L-1 氢氧化钠溶液等体积混合,反应后溶液恰好显中性, 用 a、b 表示醋酸的电离常数为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K时,各反应的平衡常数如下:
①N2(g)+O2(g)![]() 2NO(g),K=1×10-30;
2NO(g),K=1×10-30;
②2H2(g)+O2(g)![]() 2H2O(g),K=2×1081;
2H2O(g),K=2×1081;
③2CO2(g)![]() 2CO(g)+O2(g),K=4×10-92
2CO(g)+O2(g),K=4×10-92
则常温下,NO、H2O、CO2这三个化合物分解放氧的倾向最大的是( )
A.① B.② C.③ D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置不能完成相应实验的是
A. 测定乙醇的结构式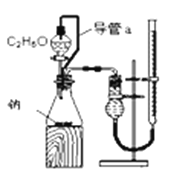
B. 验证火柴燃烧生成的SO2气体
C. 验证溴乙烷在该条件下会生成不饱和烃
D. 研究催化剂对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.检测人的血液中的葡萄糖(简称血糖,相对分子质量为180)的含量,参考指标常以两种计量单位表示,即“m mol/L”和“mg/dL”(1L=10dL).以“m mol/L”表示时,人的血糖正常值在3.61~6.11m mol/L之间。如果以“mg/dL”表示,血糖正常值范围是多少()
A. 6 mg/dL ~9mg/dL B. 55 mg/dL ~95mg/dL
C. 65 mg/dL ~110mg/dL D. 70 mg/dL ~120mg/dL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com