
| A. | 1mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| C. | 1molCl2参加的氧化还原反应,反应过程中转移电子数都是2NA | |
| D. | 常温常压下,92gNO2和N2O4混合气体含有的原子数为6NA |
分析 A.1 mol FeI2中含1mol亚铁离子和2mol碘离子;
B.铁与浓硫酸发生钝化,阻止了反应的继续进行;
C.氯气参加反应,表现性质不同,转移电子数不同,据此判断;
D.NO2和N2O4的最简式均为NO2.
解答 解:A.1 mol FeI2中含1mol亚铁离子和2mol碘离子,均能被氯气氧化为铁离子和碘单质,故1mol FeI2失去3mol电子,即3NA个,故A错误;
B.56g铁的物质的量为1mol,常温下由于铁与浓硫酸能够发生钝化,阻止了反应的进行,无法计算反应生成二氧化硫的物质的量,故B错误;
C.氯气参加反应,表现性质不同,转移电子数不同,例如氯气与水反应生成盐酸和次氯酸,Cl元素的化合价由0升高为+1价,Cl元素的化合价由0降低为-1价,1mol Cl2参加反应转移电子数为NA;1mol Cl2与铁反应生成氯化铁,氯气全部做氧化剂,1mol Cl2参加反应转移电子数为2NA,所以1mol Cl2参加反应转移电子数不一定为2NA.故C错误;
D.NO2和N2O4的最简式均为NO2,故92g混合物中含有的NO2的物质的量n=$\frac{92g}{46g/mol}$=2mol,故含6mol原子即6NA个,故D正确;
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,注意氯气做氧化剂也可以做还原剂,常温下铁在浓硫酸、浓硝酸中钝化,试题有利于提高学生灵活运用基础知识解决实际问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 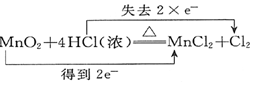 ↑+2H2O ↑+2H2O | B. | 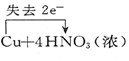 (浓)═Cu(NO3)2+2NO2↑+2H2O (浓)═Cu(NO3)2+2NO2↑+2H2O | ||
| C. | 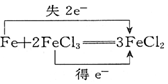 | D. | 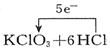 ═KCl+3Cl2↑+3H2O ═KCl+3Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 | 化学方程式 |
| ① | 将少量氯水加入盛有NaBr溶液的试管中,用力振荡后加入少量四氯化碳溶液,振荡、静置 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层变为橙红色 | Cl2+2NaBr=2NaCl+Br2 |
| ② | 将少量溴水加入盛有碘化钾溶液的试管中,用力振荡后加入少量四氯化碳溶液,振荡、静置 | 加入溴水后,溶液由无色变为褐色,滴入四氯化碳后,水层颜色变浅,四氯化碳层变为紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
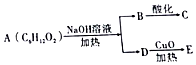
| A. | 13种 | B. | 9种 | C. | 8种 | D. | 10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将0.1mol氨充分溶解在1L水中 | |
| B. | 将10g质量分数为98%的硫酸与990g水混合 | |
| C. | 将10mL•1mol•L-1的盐酸与90mL水充分混合 | |
| D. | 将25.0g胆矾(CuSO4•5H2O)溶于水配成1L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | W | Q | |
| 10min | 1.0mol | 3.0mol | 1.0mol | 2.0mol |
| 20min | 0.5mol | 1.5mol | 2.0mol | 1.0mol |
| A. | X+2Y═2W+2Q | B. | 3X+Y+2W═2Q | C. | X+3Y+2Q═2W | D. | X+2Y+3Q═2W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在浓度大的盐酸中反应产生的气体多 | |
| B. | 一样多 | |
| C. | 在浓度小的盐酸中反应产生的气体多 | |
| D. | 由反应的剧烈程度决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
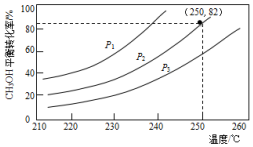 2016年9月.“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术.
2016年9月.“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFe与过量稀HNO3反应,电子转移数为2NA | |
| B. | 120g由NaHSO4和KHSO3组成的混合物含硫原子数为NA | |
| C. | 标准状况下,22.4LCH2Cl2含氯原子数为2 NA | |
| D. | 0.3mol/LAl(NO3)3溶液中含A13+数小于0.3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com