
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
A. c2一定大于0.3 mol·L-1 B. c1∶c2 一定等于1∶3
C. 平衡时,Y和Z的生成速率之比为2∶3 D. c3的取值范围为0.08<c3<0.28 mol·L-1
科目:高中化学 来源: 题型:
【题目】亚硝酸钠大量用于染料和有机合成工业。用木屑制备亚硝酸钠的流程如下:

已知:①氧化过程中,控制反应液的温度在55~60℃,发生的主要反应为C6H12O6+12HNO3![]() 3H2C2O4+9NO2↑+3NO↑+9H2O;
3H2C2O4+9NO2↑+3NO↑+9H2O;
②NaNO2有氧化性,在酸性条件下能把I-氧化为I2;S2O32-能把I2还原为I-
③NaNO2也有还原性,能使酸性KMnO4溶液褪色
(1)酸溶过程中,发生的主要反应的化学方程式为______________。
(2)实验室模拟氧化和吸收过程的装置(加热和仪器固定裝置已略去)如下图所示

①实验装置图中仪器a的名称为______________。
②A装置须控制反应液的温度不高于60℃的原因是_____________。
③B装置用于制备亚硝酸钠,其中盛放的溶液是__________(填字母)。
a.NaCl溶液 b.Na2CO3溶液 c.NaNO3溶液
(3)工业上在吸收过程中需控制NO和NO2的物质的量比接近1:1。若n(NO):n(NO2)>l:1,则会导致________;若n(NO):n(NO2)<1:1,则会导致________。
(4)为测定产品NaNO2的纯度,请补充完整实验方案:准确称量适量的NaNO2样品放入锥形瓶中,加适量水溶解,________。(实验中可供选择的试剂:稀硫酸、淀粉溶液、酚酞试液、c1mol/LKI溶液、c2mol/LNa2S2O3溶液、c3mol/L酸性KMnO4溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个12C原子的质量为a kg,一个12C16O2分子的质量为b kg,若以12C16O2中的一个氧原子质量的 ![]() 作为相对原子质量标准,则12C16O2的相对分子质量为( )
作为相对原子质量标准,则12C16O2的相对分子质量为( )
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过硫酸氢钾复盐(化学式表示为K2SO4·KHSO4·2KHSO5),—般用作漂白剂及NOx、SO2等废气脱除剂。制备过硫酸氢钾复盐流程如图:

(1)在“转化”操作前,需先用冰水冷却双氧水,可能的原因是________________。“转化”过程中,浓硫酸与H2O2发生可逆反应生成过硫酸(H2SO5),写出该变化的化学反应方程式____________________。
(2)已知H2SO5为一元强酸。结晶操作中,加入K2CO3即可获得过硫酸氢钾复盐晶体,该过程的离子反应方程式为________________________;操作中,选用50%K2CO3溶液且需分批缓慢加入目的是____________。过硫酸氢钾复盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如图所示。则该过程适宜的条件是________________。

(3)过滤后,用无水乙醇取代蒸馏水洗涤沉淀,目的是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是化学研究的基础。下列关于各实验装置的叙述正确的是( )

A. 装置①常用于分离互不相溶的液体混合物
B. 装置②可用于吸收NH3或HCl气体,并防止倒吸
C. 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
D. 装置③可用于收集H2、CO2、Cl2、NH3等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验某溶液中是否含有常见的四种无机离子,某化学小组的同学进行了如下所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得出的正确结论是( )

A.原溶液中一定含有SO42- B.原溶液中一定含有NH4+
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)H2SO4的摩尔质量为;0.3mol的NH4+中含有个电子;
(2)①标准状况下22.4L CH4 ②1.5mol NH3 ③1.806×1024个H2O ④标准状况下73g HCl所含H原子个数由多到少的顺序为(填序号);
(3)在含0.4mol Al2(SO4)3的溶液中SO42﹣的物质的量为;
(4)某常见气体在标准状况下的密度为1.25g/L,若该气体的分子式为A2型,则其名称是;
(5)取100mL a mol/L HCl溶液与300mL n mol/L H2SO4溶液均注入到500mL的容量瓶中,加水稀释到刻度线,则该混合溶液中H+的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 3Cl2 + 6KOH 5KCl + KClO3+ 3H2O中,氧化剂与还原剂的质量之比是
A. 1︰1 B. 1︰5 C. 5︰1 D. 3︰2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝合金投入100mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示. 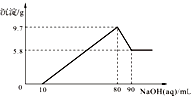
(1)当沉淀达到最大值时,Al(OH)3的质量;
(2)原合金中Mg的质量;
(3)盐酸的物质的量浓度.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com