


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源:山东省聊城三中2009-2010学年高二下学期第四次阶段性测试化学试题 题型:022
水的电离平衡曲线如图所示.
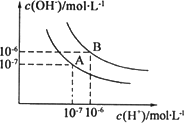
(1)若以A点表示25℃时水的电离平衡的离子浓度,当温度升高到100℃时,水的电离平衡状态移动到B点,则此时水的离子积从________变化到________.
(2)将PH=8的Ba(OH)2溶液与PH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液的PH=7,则Ba(OH)2和盐酸的体积之比为________.
(3)已知AnBm的离子积为[c(Am+)]·[c(Bn-)]m若某温度下Ca(OH)2的溶解度为0.74 g,设饱和溶液的密度为1 g/mL,其离子积约为________.
(4)已知25℃时,0.1 L 0.1 mol·L-1的NaA溶液的pH=10,则NaA溶液中所存在的离子的物质的量浓度由大到小的顺序为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
A.HA溶液的pH一定为1 B.盐MA可能水解
C.HA物质的量浓度一定为0.1mol·L-1 D.混合后的溶液中c(M+)一定等于c(A-)
查看答案和解析>>
科目:高中化学 来源:2015届山东省高二上学期期中考试化学试卷(解析版) 题型:填空题
已知MOH为一元弱碱,25℃时,电离常数 Kb= 1×10- 6 mol·L-1,
(1)25℃时,将0.2 mol·L-1 HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,此时混合溶液中由水电离出的c(H+)=Amol·L-1,若0.2 mol/L HCl溶液中由水电离出的c(H+)=Bmol·L-1,则:
①比较A B。(填“>”、“<”或“=”)
②根据电荷守恒,计算混合溶液中c(Cl-)-c(M+)=______ mol·L-1。 (精确计算,填具体数字)
(2)25℃时,0.01 mol·L-1 MOH溶液的 pH=10,将其与等体积 pH = 4的盐酸溶液混合,则混合溶液的pH 7(填“>”、“<”或“=”),试求此时溶液中M Cl的水解平衡常数Kh= mol/L
查看答案和解析>>
科目:高中化学 来源:江苏期中题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com