
| 侯氏制碱法 | 人工合成胰岛素 | 用青蒿素治疗疟疾 | 独创无氰电镀新工艺 |
 |  |  |  |
| A.以NH3、CO2、NaCl为原料最终制得纯碱 | B.由有机小分子合成有机高分子 | C.用萃取原理从青蒿素中提取青蒿素 | D.以铜盐、碱等溶液为电解质镀铜 |
| A. | A | B. | B | C. | C | D. | D |
分析 化学变化为有旧化学键的断裂和新化学键的形成,发生了化学反应,物理变化为没有新物质的生成,
A、以NH3、CO2、NaCl为原料最终制得纯碱,发生了化学反应,为化学变化;
B、由有机小分子合成有机高分子是通过加聚反应或缩聚反应实现,为化学反应;
C、萃取利用的是物质的溶解性,溶质在互不相溶的溶剂中的溶解度不同,实现物质的分离,为物理变化;
D、电镀为化学变化,以此解答.
解答 解:A.以NH3、CO2、NaCl为原料最终制得纯碱,有新物质生成,发生了化学反应,为化学变化,故A错误;
B.由有机小分子合成有机高分子是通过加聚反应或缩聚反应实现,为化学变化,故B错误;
C.萃取利用的是物质的溶解性,溶质在互不相溶的溶剂中的溶解度不同,实现物质的分离,为物理变化,故C正确;
D.电镀为铜离子得电子生成铜单质,发生了化学变化,故D错误.
故选C.
点评 本题考查物理变化与化学变化的基本概念,侧重于学生对概念的辨析能力的考查,难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验现象 | 结论或推论 | |
| A | 溴水中加入甲苯,振荡 | 水层几乎呈无色 | 甲苯与溴发生了反应 |
| B | 一小粒金属钠投入无水乙醇中 | 最后钠浮在液面上 | 密度:乙醇大于钠 |
| C | Fe(SCN)3溶液中滴入足量NaOH溶液 | 澄清后得到无色溶液 | Fe(OH)3悬浊液中滴加KSCN溶液后不显红色 |
| D | 在含Mn2+的草酸溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液褪色较快 | 反应过程中,Mn2+一定氧化了草酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
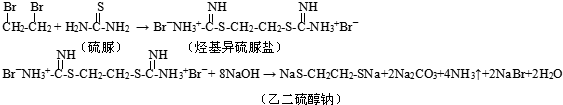
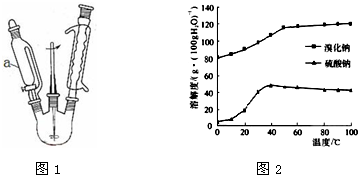
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30 g乙烷中所含的极性共价键数为7NA | |
| B. | 常温常压下,28g乙烯与丁烯的混合气体含有的碳原子数目NA | |
| C. | 密闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA | |
| D. | 标准状况下,22.4L HF含有的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
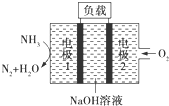
| A. | 电池工作时,Na+向电极1移动 | |
| B. | 电池工作一段时间后停止,溶液pH值不变 | |
| C. | 电极1发生的电极反应为2NH3+6OH--6e-═N2↑+6H2O | |
| D. | 用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某芳香烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有3种 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次降低 | |
| C. | 肌醇 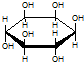 与葡萄糖 与葡萄糖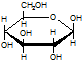 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 | |
| D. | 1.0 mol的有机物(结构如图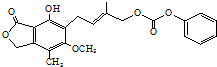 )最多能与含5.0 mol NaOH的水溶液完全反应 )最多能与含5.0 mol NaOH的水溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
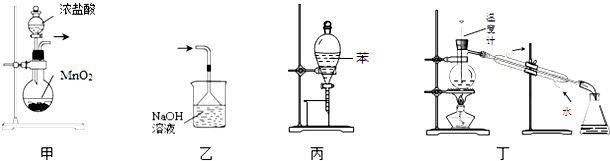
| A. | 用装置甲制取氯气 | B. | 用乙装置除去氯气中的HCl气体 | ||
| C. | 用丙装置萃取溴水中的溴单质 | D. | 用丁装置分离乙酸与乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
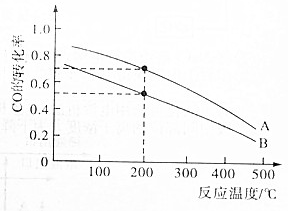 高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题.
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+2H2(g)?CH3OH(g).请根据图示回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com