
| A. | 粗铜作阴极? | |
| B. | 用CuSO4作电解质溶液 | |
| C. | 阳极只发生Cu-2e-═Cu2+反应,其它杂质沉淀为阳极泥 | |
| D. | 电解质溶液的组成和浓度都不改变? |
分析 电解法精炼铜时,粗铜为阳极,精铜为阴极,电解质溶液为硫酸铜,阳极材料是粗铜,阳极上失电子变成离子进入溶液,Cu-2e-=Cu2+,比金属铜活泼的金属锌、铁、镍会先于金属铜失电子,比金属铜活泼性差的Pt、Ag等固体会沉积下来形成阳极泥,根据电解原理来回答.
解答 解:A、电解法精炼铜时,粗铜为阳极,精铜为阴极,故A错误;
B、电解法精炼铜时,粗铜为阳极,精铜为阴极,电解质溶液为硫酸铜溶液,故B正确;
C、阳极上失电子变成离子进入溶液,Cu-2e-=Cu2+,比金属铜活泼的金属锌、铁、镍会先于金属铜失电子,比金属铜活泼性差的Pt、Ag等固体会沉积下来形成阳极泥,故C错误;
D、阳极上失电子变成离子进入溶液,Cu-2e-=Cu2+,比金属铜活泼的金属锌、铁、镍会先于金属铜失电子,阴极上始终是铜离子的电子的还原反应,所以电解质溶液的组成和浓度都变化,故D错误.
故选B.
点评 本题考查学生电解精炼铜的工作原理,把握阳极、阴极材料及电极反应为解答的关键,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
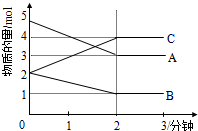 (1)某可逆反应(ABC均为气体)从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.
(1)某可逆反应(ABC均为气体)从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 编号 | 装置缺陷和不妥之处 |
| ① | |
② | |
③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com